Изменение - концентрация - электролит
Cтраница 2
Благодаря чувствительности к изменению концентрации электролитов в золе электрокипетический потенциал играет большую роль для характеристики состояния различных гидрофобных систем. Во всех электрокинетичсских явлениях ( электроосмос, электрофорез) ему принадлежит ведущая роль. Таким образом, дзета-потенциал является одним из важнейших факторов устойчивости гидрофобных золен. Опыт показывает, что чем больше величина этого потенциала, тем более устойчива коллоидная система. [16]
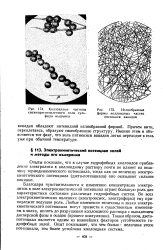 |
Коллоидные частицы свежеприготовленного золя сульфида мышьяка. [17] |
Благодаря чувствительности к изменению концентрации электролитов в золе электрокинетитеский потенциал играет большую роль для характеристики состояния различных гидрофобных систем. Во всех электрокинетических явлениях ( электроосмос, электрофорез) ему принадлежит ведущая роль. Таким образом, дзета-потенциал является одним из важнейших факторов устойчивости гидрофобных золей. Опыт показывает, что чем больше величина этого потенциала, тем более устойчива коллоидная система. [18]
Концентрационная поляризация вызывается изменением концентрации электролита у электродов по сравнению с концентрацией в глубине раствора. Например, при пропускании тока ионы Си2 разряжаются на катоде и их концентрация у катода уменьшается по сравнению с концентрацией в глубине раствора. [19]
Скорость нагрева регулируется изменением концентрации электролита и напряжения тока. Время нагрева зависит от скорости вращения диска. [20]
Концентрационная поляризация возникает вследствие изменения концентрации электролита в катодном и анодном пространствах по мере электролиза. [21]
Концентрационная поляризация возникает вследствие изменения концентрации электролита в катодном и анодном пространствах по мере электролиза. [22]
В процессе электролиза происходят изменения концентрации электролита, которые обусловлены участием ионов в переносе тока, химическими процессами, протекающими на электродах и в объеме электролита, испарением влаги и уносом ее с газообразными продуктами электролиза - хлором и водородом. [23]
 |
Мост Кольрауша с ячейкой для определения электропроводности. [24] |
Измерение электропроводности позволяет изучить изменение концентрации электролитов в сыворотке крови при патологических состояниях. Электропроводность значительно меняется с изменением температуры, поэтому ее нужно измерять при постоянной температуре. [25]
В процессе титрования происходит изменение концентрации электролитов и электропроводности раствора в ячейке титрования за счет осаждения сульфата бария. [26]
В процессе титрования происходит изменение концентрации электролитов и электропроводности раствора в ячейке титрования за счет осаждения сульфата бария и вводимого избытка хлорида бария. Это вызывает изменение соггоотивления высокочастотного датчика, которое фиксируется стрелкой прибора. [27]
При вычислении чисел переноса изменения концентрации Электролита у электродов и общее изменение концентрации, конечно, должны быть выражены в одних и тех же единицах, например, в грамм-эквивалентах электролита. [28]
 |
Метод подвижной границы для определения чисел переноса.| Метод Гитторфа по определению чисел переноса. [29] |
Числа переноса определяются по изменениям концентрации электролита в анодном и катодном пространствах. [30]
Страницы: 1 2 3 4