Микропористое стекло
Cтраница 3
Спектры ряда соединений ( например, бензола, нафталина, 1 2 4 5-тетрахлорбензола) при сравнительно малых заполнениях поверхности почти не отличались от спектра той конденсированной фазы, которая существует при комнатной температуре. Например, в СКР бензола на поверхности микропористого стекла при заполнениях 0.5 - 0.7 слоя появляется линия 1475 см 1, запрещенная в СКР паров СвН6 вследствие альтернативного запрета. [31]
В спектрах некоторых соединений ( SbQ3, SbBr3, дихлорэтана и др.) в адсорбированном состоянии при малых заполнениях наблюдаются изменения частот и интенсивностей в отдельных областях или всего спектра по сравнению со спектром конденсированной фазы при комнатной температуре. Так в СКР SbCl3, адсорбированной на микропористом стекле при заполнениях, начиная примерно с 0.1 слоя, на месте линий валентных и деформационных колебаний кристаллической 8ЬС13 появляются две полосы полушириной 50 - 70 см 1 с несимметричными контурами, максимумы которых смещены относительно линий валентных и деформационных колебаний. Такие же изменения в спектрах наблюдаются при адсорбции на силикагеле и алюмосиликагеле, в последнем случае спектры еще более размыты. [32]
Это может быть истолковано так, что в данной области составов бор переходит из состояния I в состояние II, оставаясь в. С таким выводом прекрасно согласуется известный факт существования микропористых стекол. Составы последних как раз характеризуются низким соотношением Na2O / B2O3, не превышающим обычно Vs. Бор, находящийся в тройной координации, является химически нестойкой составной частью и легко вымывается из стекла кислотами вместе со связанной с ним окисью натрия. В остатке сохраняется неповрежденным почти чистый пористый скелет кремнезема с незначительной примесью щелочи. [33]
Нам кажется, что в настоящее время имеются экспериментальные данные, которые говорят в пользу первой точки зрения. Рассмотрим это на примере адсорбции молекул воды на микропористом стекле и различных силикагелях. В работе [4] было показано, что первые порции воды адсорбируются на силикагеле с теплотой адсорбции 17 - 20 ккал / молъ. Это показывает, что адсорбция происходит не по механизму водородной связи; здесь имеют дюсто связи более сильные, чем водородные. В работе Йетса [5] было показано, что при адсорбции молекул, способных вступить в водородную связь с ОН-группами поверхности, наблюдается значительное уменьшение ( сжатие) размеров адсорбента, которое объясняется образованием водородной связи на поверхности. Адсорбция первых порций молекул воды не приводит к уменьшению размеров адсорбента и лишь последующая адсорбция приводит к сжатию. Авторы приходят к выводу, что адсорбция большинства молекул при малых заполнениях происходит без образования водородных связей. Анализ спектров ЯМР [4, 6] также показывает, что в области малых заполнений вода адсорбируется на силикагеле на других более активных центрах. Как было показано в работах Сидорова [7, 8], свободные ОН-группы поверхности пористого стекла не являются центрами адсорбции по отношению к молекулам воды и вода на дегидратированной поверхности адсорбируется на каких-то других центрах, названных ( в отличие от ОН-групп) центрами второго рода. [34]
Нам кажется, что в настоящее время имеются экспериментальные данные, которые говорят в пользу первой точки зрения. Рассмотрим это на примере адсорбции молекул воды на микропористом стекле и различных силикагелях. В работе [4] было показано, что первые порции воды адсорбируются на силикагеле с теплотой адсорбции 17 - 20 ккал / молъ. Это показывает, что адсорбция происходит не по механизму водородной связи; здесь имеют место связи более сильные, чем водородные. В работе Йетса [5] было показано, что при адсорбции молекул, способных вступить в водородную связь с ОН-группами поверхности, наблюдается значительное уменьшение ( сжатие) размеров адсорбента, которое объясняется образованием водородной связи на поверхности. Адсорбция первых порций молекул воды не приводит к уменьшению размеров адсорбента и лишь последующая адсорбция приводит к сжатию. Авторы приходят к выводу, что адсорбция большинства молекул при малых заполнениях происходит без образования водородных связей. Анализ спектров ЯМР [4, 6] также показывает, что в области малых заполнений вода адсорбируется на силикагеле на других более активных центрах. Как было показано в работах Сидорова [7, 8], свободные ОН-группы поверхности пористого стекла не являются центрами адсорбции по отношению к молекулам воды и вода на дегидратированной поверхности адсорбируется на каких-то других центрах, названных ( в отличие от ОН-групп) центрами второго рода. [35]
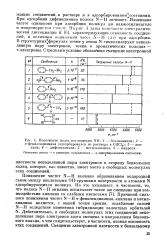 |
Положение полос поглощения NH. 1 - бснзиламина. 2 - n - фенилендиамина ( адсорбировался из раствора в СНС13. 3 - анилина. 4 - дифениламина. 5 - метиланилина. 6 - пиррола. [36] |
При адсорбции дифениламина полоса N - Н исчезает. Изменение частот одинаково при адсорбции молекул на алюмосиликагеле и микропористом стекле. На рис. 4 даны константы электролитической диссоциации К [6], характеризующие основность соединений, и величины понижения часе. В структурных формулах точки у атома N символизируют неподеленную пару электронов, точки в ароматических кольцах - тт-электроны. [37]
В первом случае в качестве матрицы обычно используют целлюлозу, декстраиовые гели ( сефарозу, агарозу), микропористые стекла или кремнеземы, а также синтетич. Матрицу при ковалентной иммобилизации ферментов обычно предварительно активируют, обрабатывая, напр. Благодаря этому она становится носителем активных группировок, к-рые способны вступать в р-цию сочетания, взаимод. Во втором случае в качестве гелеобразующего полимера используют полиакриламид. [38]
В последние годы большое внимание в физике конденсированной среды уделено исследованию процессов переноса в материалах с неупорядоченной структурой - жидкостях, стеклах, сильно легированных полупроводниках, неоднородных проводниках. Примерами последних могут служить сильно спрессованные смеси проводящих и непроводящих материалов; двухфазные системы, в которых одна фаза обладает значительно большей проводимостью, нежели другая; микропористые стекла, поры которых заполнены различными веществами. [39]
Водородная связь в этом случае обусловлена в основном электростатическими взаимодействиями. Полоса поглощения 3720 см-1 соответствует основной частоте колебаний ОН скелетных гидроксилов. Кривая 2 представляет собой ИК-спектр исходного микропористого стекла после контактирования со ш стиролом. В этом случае полоса поглощения ОН-групп также смещена в сторону меньших частот и значительно расширена, благодаря чему можно сделать вывод об образовании водородной связи. [40]
В настоящей работе в области спектра 5500 - 9000 см 1 исследовались изменения, наступающие в первых обертонах валентных колебаний ряда органических молекул при их адсорбции из растворов в СС14 на поверхности алюмосиликагеля ( синтетического катализатора) и силика-геля. Эти изменения были сравнены с изменениями полосы ОН-групп микропористого стекла при адсорбции тех же соединений из газовой фазы. [41]
Мембраны из микропористого стекла. Стеклянные мембраны обладают такими ценными свойствами, как высокая термическая и химическая стойкость, неподверженность действию микроорганизмов и жесткость структуры. Эти свойства позволяют использовать их при разделении растворов в широком интервале рН ( 1 - 10) и проводить стерилизацию. Мембраны из микропористого стекла могут быть изготовлены в виде пластин, пленок, трубок или капилляров. [42]
Страницы: 1 2 3