Степень - диссоциация - слабая кислота
Cтраница 1
Степень диссоциации слабой кислоты в присутствии ее соли сильно понижается. [1]
 |
Константы ионизации некоторых кислородсодержащих кислот.| Сильные водорастворимые кислоты, образуемые оксианионами. [2] |
Степень диссоциации слабых кислот обычно поддается измерению гораздо легче. О кислотности слабых кислородсодержащих кислот можно судить по их константе ионизации в водных растворах; подобные данные приводятся в табл. 20.5. В этом случае также прослеживается закономерная связь между ионным потенциалом гипотетического центрального иона и силой кислоты. [3]
Так как степень диссоциации слабых кислот возрастает пропорционально температуре, то хлоргидринирование при повышенных температурах идет, в принципе, хуже. [4]
Последние лишь снижают степень диссоциации слабых кислот и оснований, которые в незаряженном состоянии значительно легче проникают в клетки, чем продукты их диссоциации. Физиологически активны всегда именно недиссоциированные кислоты. Двухосновная янтарная кислота или трехосновная лимонная тем скорее проникает в клетку, чем ниже рН среды. [5]
Подобным способом понижения степени диссоциации слабых кислот и оснований нередко пользуются при анализе. [6]
Однако при вычислениях степени диссоциации слабых кислот и оснований в их очень разбавленных водных растворах необходимо учитывать влияние на этот процесс концентрации водородных или гидроксильных ионов, образующихся в результате диссоциации самой воды. [7]
Задача сводится к определению степени диссоциации слабой кислоты в растворе с фиксированной концентрацией водородных ионов. [8]
Степень гидролиза по аниону зависит от степени диссоциации слабой кислоты. [9]
Неполярные растворители ( например, диоксан) уменьшают степень диссоциации слабых кислот, увеличивая различие в константах диссоциации, и, следовательно, улучшают разделение. Использование органических растворителей приводит к подавлению сорбции недиссоциированных молекул, что уменьшает четкость разделения. [10]
Рассмотрим, какое влияние оказывает присутствие сильной кислоты на степень диссоциации слабой кислоты, на примере соляной и уксусной кислот. [11]
При поглощении смолой ( анионитом) в гидроксильной форме цианидов из нейтральных или слабокислых растворов решающим фактором процесса служит степень диссоциации слабой кислоты ( какой, в частности, является синильная кислота) и степень диссоциации функциональных групп смолы. [12]
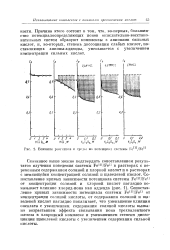 |
Влияние реагентов и среды нп потенциал системы Fe / Fe. [13] |
Причина этого состоит в том, что, во-первых, большинство потенциалоопределяющих ионов окислительно-восстановительных систем образуют комплексы с анионами сильных кислот, и, во-вторых, степень диссоциации слабых кислот, поставляющих анионы-адденды, уменьшается с увеличением концентрации сильных кислот. [14]
При нейтрализации слабой кислоты сильным основанием или, наоборот, сильной кислоты слабым основанием тепловой эффект нейтрализации может быть меньше или больше 57 1 - 103 дж. Степень диссоциации слабых кислот и оснований небольшая, и процесс титрования сопровождается диссоциацией слабой кислоты ( основания) на ионы. Процесс же диссоциации разных электролитов имеет различный тепловой эффект диссоциации как по величине, так и по знаку. [15]
Страницы: 1 2