Степень - диссоциация - вещество
Cтраница 3
Полученные соотношения позволяют сделать ряд заключений относительно влияния степени диссоциации веществ на возможность образования резкой границы зон ионов при обмене ионов не полностью диссоциированных веществ в динамических условиях. При обмене ионов равной валентности, как следует из уравнения ( II, 41), уменьшение степени диссоциации десорбируемых веществ и увеличение степени диссоциации десорбирующих веществ приводит к повышению вероятности образования резкого фронта между вытеснителем и вытесняемым веществом. При обмене ионов разной валентности степени диссоциации десорбирующего и десор-бируемого вещества также играют очень большую роль. [31]
Согласно теории динамики ионообменной сорбции [13, 14], поиски условий обострения границ зон ионов при обмене ионов равной валентности могут быть основаны не только на изменении константы ионного обмена, но и на изменении степени диссоциации веществ, образующих в растворе обменивающиеся ионы. Вероятность образования резкой границы между зонами ионов повышается при уменьшении степени диссоциации веществ, образующих вытесняемые ионы, или при увеличешги степени диссоциации веществ, образующих ионы-вытеснители. В случае обмена ионов антибиотиков группы тетрациклина не представляет труда выбрать условия, когда степень диссоциации антибиотиков с образованием катионов была бы достаточно мала, а степень диссоциации веществ, образующих катионы-вытеснители, была бы большой. Для этого необходимо проводить десорбцию антибиотиков с сульфосмол растворами щелочей. Однако малая стабильность антибиотиков в щелочных растворах делает целесообразным применение растворов со значением рН, не превосходящим 10 - И. [32]
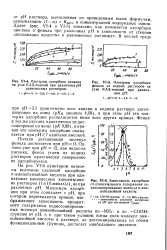
Далее ( рис, VI-4 и VI-5) показано, как изменяется адсорбция анилина и фенола при различных рН в зависимости от степени диссоциации вещества в равновесных растворах. [34]
При помощи простого и дешевого оборудования использование электрофореза на бумаге позволяет разделять редкоземельные элементы, белки, нуклеиновые кислоты и другие соединения, входящие в состав живых и растительных организмов, также разделять смеси радиоактивных веществ. На движение частиц в электрическом поле влияют такие факторы, как знак и величина ионов, или коллоидных частиц, присутствие комплексообразователей, изменяющих тип и степень диссоциации вещества. [35]
Электрическая проводимость растворов электролитов зависит от общего числа их ионов в единице объема раствора. Вследствие этого удельная электрическая проводимость электролитов зависит от концентрации раствора; по мере увеличения концентрации сначала растет, а затем уменьшается, так как вместе с ростом числа ионов уменьшается скорость их перемещения, а также степень диссоциации вещества. Первый фактор действует в растворах сильных электролитов, второй - в растворах слабых электролитов. [36]
Полученные соотношения позволяют сделать ряд заключений относительно влияния степени диссоциации веществ на возможность образования резкой границы зон ионов при обмене ионов не полностью диссоциированных веществ в динамических условиях. При обмене ионов равной валентности, как следует из уравнения ( II, 41), уменьшение степени диссоциации десорбируемых веществ и увеличение степени диссоциации десорбирующих веществ приводит к повышению вероятности образования резкого фронта между вытеснителем и вытесняемым веществом. При обмене ионов разной валентности степени диссоциации десорбирующего и десор-бируемого вещества также играют очень большую роль. [37]
Что касается первичного солевого эффекта, то его можно объяснить лишь на основании теории сильных электролитов Дебая - Гюккеля ( см. гл. Введение соли, не содержащей общих ионов с компонентами смеси, изменяет ионную силу ( см. гл. XVIII, § 17) раствора, вследствие чего изменяются степени диссоциации веществ и концентрации катализирующих реакцию частиц. [38]
Согласно теории динамики ионообменной сорбции [13, 14], поиски условий обострения границ зон ионов при обмене ионов равной валентности могут быть основаны не только на изменении константы ионного обмена, но и на изменении степени диссоциации веществ, образующих в растворе обменивающиеся ионы. Вероятность образования резкой границы между зонами ионов повышается при уменьшении степени диссоциации веществ, образующих вытесняемые ионы, или при увеличешги степени диссоциации веществ, образующих ионы-вытеснители. В случае обмена ионов антибиотиков группы тетрациклина не представляет труда выбрать условия, когда степень диссоциации антибиотиков с образованием катионов была бы достаточно мала, а степень диссоциации веществ, образующих катионы-вытеснители, была бы большой. Для этого необходимо проводить десорбцию антибиотиков с сульфосмол растворами щелочей. Однако малая стабильность антибиотиков в щелочных растворах делает целесообразным применение растворов со значением рН, не превосходящим 10 - И. [39]
Для создания резкой границы между зонами иона-вытеснителя и вытесняемого иона в случае обмена равно-валентных ионов необходимо таким образом подбирать систему, чтобы константа обмена в уравнении ( II, 29) была больше единицы, когда первым ионом является ион-вытеснитель. Это осуществимо при сорбции ионов, энергия взаимодействия которых с сорбентом больше, чем энергия взаимодействия с ионом, ранее находившимся на ионите ионов. При обмене разновалентных ионов существенное значение имеет концентрация вводимого в колонку сорбируемого иона. Наконец, изменение степени диссоциации веществ путем изменения рН среды является одним из важнейших факторов, позволяющих создавать условия, благоприятные для сорбции и вытеснения ионов. Нельзя не отметить значения свойств растворителей, которые оказывают влияние и на константу ионного обмена, и на степень диссоциации веществ. Рациональный выбор условий проведения сорбционных процессов позволил, как будет показано дальше, построить ряд эффективных методов выделения и очистки антибиотиков. [40]
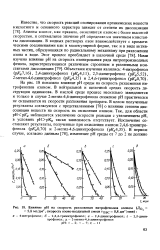 |
Влияние рН на скорость разложения нитрофенолов озоном СДо3. [41] |
На рис. 18 показано влияние рН среды на скорость разложения ни-трофенолов озоном. В нейтральной и щелочной средах скорость деструкции одинакова. В кислой среде процесс несколько замедляется и только в случае 2-метил - 4 6-динитрофенола снижение рН практически не сказывается на скорости разложения препарата. В целом полученные результаты согласуются с представлениями [78] о влиянии степени диссоциации веществ на скорость их окисления озоном. Так, для области рНрА а наблюдается увеличение скорости реакции с увеличением рН, в условиях рНрКд такая зависимость отсутствует. [42]
Для создания резкой границы между зонами иона-вытеснителя и вытесняемого иона в случае обмена равно-валентных ионов необходимо таким образом подбирать систему, чтобы константа обмена в уравнении ( II, 29) была больше единицы, когда первым ионом является ион-вытеснитель. Это осуществимо при сорбции ионов, энергия взаимодействия которых с сорбентом больше, чем энергия взаимодействия с ионом, ранее находившимся на ионите ионов. При обмене разновалентных ионов существенное значение имеет концентрация вводимого в колонку сорбируемого иона. Наконец, изменение степени диссоциации веществ путем изменения рН среды является одним из важнейших факторов, позволяющих создавать условия, благоприятные для сорбции и вытеснения ионов. Нельзя не отметить значения свойств растворителей, которые оказывают влияние и на константу ионного обмена, и на степень диссоциации веществ. Рациональный выбор условий проведения сорбционных процессов позволил, как будет показано дальше, построить ряд эффективных методов выделения и очистки антибиотиков. [43]
Страницы: 1 2 3