Степень - диссоциация - растворенное вещество
Cтраница 2
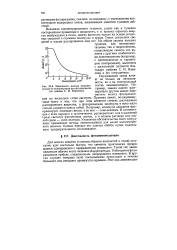 |
Зависимость выхода люминесценции от концентрации для флуоресцеина ( по данным С. И. Вавилова. [16] |
Причина лежит, по-видимому, чаще всего в том, что при этом меняется степень диссоциации растворенного вещества, а флуоресценции молекулы и иона часто сильно разнятся между собой. Например, молекула акридина флуоресцирует лиловым светом, а ее ион - сине-зеленым. В соответствии с этим акридин в органических растворителях или в щелочной реде светится фиолетовым светом, а в водном растворе или кислой среде - сине-зеленым. Указанные обстоятельства часто затрудняют применение метода люминесценции для целей количественного анализа. Однако нередко это удается обойти путем тщатель-нбго предварительного исследования. [17]
В некоторых случаях, особенно в водных растворах, явление концентрационного тушения осложняется физршо-химическими явлениями - изменением степени диссоциации растворенного вещества или ассоциацией молекул с образованием димеров или более сложных ассоциатов. При этом часто димеризованные молекулы не обладают люминесценцией ( иногда спектр люминесценции у них иной, чем у мономеров), и уменьшение выхода в таких случаях может быть обусловлено двумя причинами. Во-первых, нелюминесцирующиедимерымогут давать эффект светофильтра, о котором говорилось выше, и, во-вторых, возможен резонансный перенос энергии от возбужденных простых молекул к димеризованным. [18]
Верхний предел концентрации электролитов, допускающий получение надежных данных с помощью этого метода, определяется в основном степенью диссоциации растворенного вещества и частотой, при которой проводятся измерения. Если 1 превышает 5 10 - 3, то возникают всевозрастающие трудности в определении положения минимумов с достаточной степенью точности. [19]
Раствор, содержащий 10 - 3 кг нелетучего вещества с молекулярной массой 186 в 0 1 кг воды, замерзает на 0 10 ниже температуры замерзания растворителя. Определите степень диссоциации растворенного вещества, учитывая, что каждая его молекула в растворе может распадаться на три частицы. [20]
Увеличение осмотического давления по сравнению с заданной концентрацией вещества в i раз связано с увеличением числа частиц в растворе электролитов вследствие процесса электролитической диссоциации и, как показал С. Аррениус, зависит от степени диссоциации растворенного вещества а в данном растворителе. [21]
 |
Распределение аммиака между на мысль том что эти Два процесса, водой и газовой фазой. вероятно, тесно связаны друг с дру. [22] |
Генри в этом случае не применим. Независимые кондуктометрические измерения позволяют определить степень диссоциации растворенного вещества а. Следующий вопрос заключается в том, является ли выражение р / с у. [23]
Следует иметь в виду, что величина а, а следовательно, и i зависят от температуры, и поэтому найденный коэффициент Вант-Гоффа имеет смысл только для температуры, при которой выполнены измерения. При переходе от одного растворителя к другому степень диссоциации растворенного вещества изменяется, а следовательно, изменяется и коэффициент Вант-Гоффа. Этот метод рассматривается в электрохимии. [24]
Следует иметь в виду, что величина а, а следовательно, и i зависят от температуры, и поэтому найденный коэффициент Вант-Гоффа имеет смысл только для температуры, при которой выполнены измерения. При переходе от одного растворителя к другому степень диссоциации растворенного вещества изменяется, а следовательно, изменяется и коэффициент Вант-Гоффа. [25]
Вопрос о том, по какому из этих соотношений рассчитывать осмотический коэффициент для характеристики реальной системы, должен решаться для каждой конкретной системы отдельно. Необходимо только отметить, что для расчета осмотического коэффициента в последнем случае необходимо знать степень диссоциации растворенного вещества. [26]
Осмотическое давление почвенного раствора имеет важное значение для растений. Если оно равно или выше осмотического давления клеточного сока растений, то поступление воды в растение прекращается, и оно погибает. Осмотическое давление зависит от концентрации почвенного раствора и степени диссоциации растворенных веществ. [27]
Дандон и Мак [173] считают, что формула Джонса слишком громоздка. Кроме того, в связи с тем, что незначительным изменениям степени диссоциации растворенного вещества соответствуют большие изменения в концентрации, даже малые ошибки в определении степени диссоциации могут в конечном итоге привести к большим ошибкам в определении концентрации. [28]
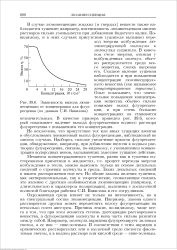 |
Зависимость выхода люминесценции от концентрации для флуо-ресцеина ( по данным С.И. Вавилова. [29] |
Окружающая среда влияет не только на интенсивность, но и на спектральный состав люминесценции. Например, замена одного растворителя другим может переместить полосу флуоресценции на несколько сотен ангстрем. Причина лежит, по-видимому, чаще всего в том, что при этом меняется степень диссоциации растворенного вещества, а флуоресценции молекулы и иона часто сильно разнятся между собой. Например, молекула акридина флуоресцирует лиловым светом, а ее ион - сине-зеленым. В соответствии с этим акридин в органических растворителях или в щелочной среде светится фиолетовым светом, а в водном растворе или кислой среде - сине-зеленым. [30]
Страницы: 1 2 3