Степень - диссоциация - вода
Cтраница 1
Степень диссоциации воды ( а следовательно, константа диссоциации и ионное произведение воды) была впервые определена при помощи измерения электропроводности тщательно очищенной воды. [1]
Степень диссоциации воды при комнатной температуре а 1 8 10 - 9, что составляет очень небольшую величину. Так, из 555 600 000 молекул воды в ионизированном состоянии находится всего лишь одна. Но, принимая во внимание очень большую скорость процесса диссоциации и высокую быстроту реакций между ионами, даже малая их концентрация может обусловливать и определенным образом направлять химический процесс. В связи с этим факт диссоциации воды имеет большое значение. [2]
Степень диссоциации воды весьма мала. [3]
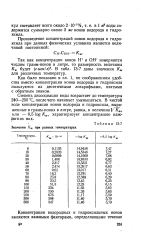 |
Значения Kw ПРИ разных температурах. [4] |
Степень диссоциации воды возрастает до температуры 240 - 250 С, после чего начинает уменьшаться. В чистой воде концентрации ионов водорода и гидроксила, выраженные в грамм-ионах в литре, равны, и величина KW, или - 0 5 log Kw, характеризует концентрацию каждого из них. [5]
Степень диссоциации воды а1 8 - 10 - 9, что составляет очень небольшую величину. Так, из 556 000 000 молекул Н2О в диссоциированном состоянии при комнатной температуре в среднем находится лишь одна. Несмотря на это, ионизация воды имеет большое значение. [6]
Степень диссоциации воды а1 8 10 - 9, что составляет очень небольшую величину. Так, из 556 000 000 молекул FbO в диссоциированном состоянии при комнатной температуре в среднем находится лишь одна. Несмотря на это, ионизация воды имеет большое значение. [7]
Степень диссоциации воды при очень высоких давлениях служила объектом многочисленных исследований. Ионное произведение активности воды Kw, измеренное при 25 С и при давлении 200 МПа, оказалось в 4 раза большим, чем при атмосферном давлении; при давлении же, равном 800 МПа, эта величина возросла в 51 3 раза. Особенно сильно возрастает Kw при одновременном действии высоких давлений и температур. Правда, в таких условиях воду уже нельзя считать жидкой фазой - давления и температуры соответствуют закритической области. [8]
Степень диссоциации воды а0, найденная из опыта, 1 2 10 - 7 г-мол. [9]
Степень диссоциации воды при комнатной температуре найдена равной а 1 8 - КГ9, что составляет очень небольшую величину. Так, из 555 600 000 молекул воды в ионизированном состоянии находится всего лишь одна. Но, принимая во внимание очень большую скорость процесса диссоциации и высокую быстроту реакций между ионами, даже малая их концентрация может обусловливать и - определенным образом направлять химический процесс. В связи с этим факт диссоциации воды имеет большое значение. [10]
Степень диссоциации воды очень мала; чистая вода практически не проводит электрический ток. [11]
Степень диссоциации воды очень мала и поэтому можно принять концентрацию недиссоциированных молекул постоянной. [12]
Поскольку степень диссоциации воды очень мала, то сн. [13]
Но степень диссоциации воды очень мала, и концентрацию ее недиссоциированных молекул в любом разбавленном водном растворе можно считать величиной постоянной. Таким образом, в правой части уравнения находятся две постоянные величины: [ Н О ] - концентрация недиссоциированных молекул воды и А - константа диссоциации. Но произведение двух постоянных величин есть также величина постоянная. [14]
 |
Схема обозначений реакции среды. [15] |
Страницы: 1 2 3 4