Степень - диссоциация - слабый электролит
Cтраница 2
Степень диссоциации слабого электролита, диссоциирующее на два иона, обратно пропорциональна корню квадратному из величины концентрации электролита в растворе. [16]
Степень диссоциации слабого электролита ( а) связана с концентрацией раствора С зависимостью, получаемой из выражения константы диссоциации К. [17]
Если степень диссоциации слабого электролита очень мала ( а С 0 05), то величину ( 1 - а) можно принять равной единице. [18]
Увеличение степени диссоциации слабого электролита с увеличением разведения находится в полном согласии с правилом Ле Шателье. [19]
Зависимость степени диссоциации слабого электролита от разведения раствора также наглядно можно показать, используя тот факт, что при равновесии скорости прямого и обратного процесса равны и равновесные концентрации находятся в простом соотношении со степенью диссоциации. [20]
Величина степени диссоциации слабых электролитов, определенная различными методами, имеет одинаковое значение. Степень же диссоциации сильного электролита, при определении ее различными методами, имеет столь различные значения, что их нельзя объяснить ошибками опыта. [21]
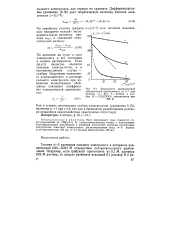 |
Зависимость эквивалентной электрической проводимости от с1 / 2 для сильных ( / - КС1, 2 - ZnS04 и слабых ( 3 - СНзСООН электролитов при 298 К. [22] |
Как и степень диссоциации слабых электролитов ( уравнение 9.13), величина / х - - 1 при с - - 0, так как в бесконечно разбавленном растворе межионное взаимодействие практически отсутствует. [23]
Как зависит степень диссоциации слабого электролита от константы диссоциации и концентрации его в водном растворе. [24]
Следовательно, степень диссоциации слабого электролита понижается при введении в раствор какого-нибудь сильного электролита с одноименным ионом. [25]
Итак, степень диссоциации слабого электролита уменьшается, если внести в раствор сильный электролит с одноименным ионом, даже если сильный электролит взят в малом количестве. Если же добавить большое количество сильного электролита, то слабый электролит становится практически недиссоциированным. Отсюда следует, что слабая кислота в присутствии собственной соли или сильной кислоты почти не распадается на ионы. То же можно сказать о слабом основании, диссоциация которого подавляется в сильнощелочной среде или в присутствии соли одноименного катиона. [26]
Итак, степень диссоциации слабого электролита уменьшается, если внести в раствор сильный электролит с одноименным ионом, даже если сильный электролит взят в малом количестве. Если же добавить большое количество сильного электролита, то слабый электролит становится практически недиссоциированным. Отсюда следует, что слабая кислота в присутствии собственной соли или сильной кислоты почти не распадается на ионы. То же можно сказать о слабом основании, диссоциация которого подавляется в сильнощелочной среде пли в присутствии соли одноименного катиона. [27]
Итак, степень диссоциации слабого электролита уменьшается, если внести в его раствор сильный электролит с одноименным ионом, даже если сильный электролит взят в малом количестве. Если же добавить большое количество сильного электролита, то слабый электролит становится практически недиссоциированным. Отсюда следует, что слабая кислота в присутствии ее соли или сильной кислоты почти не распадается на ионы. То же можно сказать о слабом основании, диссоциация которого подавляется в сильнощелочной среде или в присутствии соли одноименного катиона. [28]
Следовательно, степень диссоциации слабого электролита понижается при введении в раствор какою-нибудь сильного электролита с одноименным ионом. [29]
Так как степень диссоциации слабого электролита очень мала, то ею в знаменателе можно пренебречь. [30]
Страницы: 1 2 3 4