Степень - заполнение - поверхность - электрод
Cтраница 2
Влияние органических ингибиторов на скорость электродных процессов определяется степенью заполнения поверхности электрода молекулами ингибитора. Особый интерес представляет установление зависимости между адсорбируемостью органических веществ, степенью торможения электродного процесса и особенностями строения их молекул. [16]
И следовательно, и всего процесса в целом зависит от степени заполнения поверхности электрода адсорбированными частицами. [17]
Нам казалось, что при наличии замедленной электрохимической стадии увеличение степени заполнения поверхности электрода адсорбированными продуктами реакции должно вызвать рост перенапряжения на величину, близкую к равновесному потенциалу адсорбированного слоя, подобно тому, как это представляли А. Н. Фрумкин и Н. А. Аладжалова [6] в случае водородного перенапряжения на палладии. Учитывая приведенную выше зависимость роста перенапряжения от концентрации аниона, мы пришли к предположению о том, что увеличение окисления поверхности происходит при участии кислоты. [18]
В ехр ( - ДО / Г); 0 - степень заполнения поверхности электрода адсорбированными комплексами ( О Г / Г); а - аттракционная постоянная. [19]
Для равновесного адсо рбционно-десорбционного процесса адсорбцию вещества при заданной концентрации характеризует степень заполнения поверхности электрода молекулами или ионами адсорбата. [20]
Такое изменение величины Y в соответствии с формулой (7.79) отражает уменьшение степени заполнения поверхности электрода адсорбированным веществом-катализатором. По той же причине, а также из-за уменьшения абсолютного значения - потенциала максимум на кривой смещается в сторону положительных значений потенциала. Таким образом, закономерности процесса каталитического выделения водорода наглядно демонстрируют воздействие на поляризационные характеристики электродной реакции самых различных факторов: природы лимитирующей стадии, гомогенного или гетерогенного характера протолитической реакции (7.69), рН раствора, концентрации катализатора в растворе и его адсорбционной способности, параметров двойного электрического слоя. [22]
С увеличением плотности анодного тока и смещением потенциала в положительную сторону возрастает степень заполнения поверхности электрода окислом и толщина окисной пленки. При достижении критической анодной плотности тока поверхность электрода оказывается преимущественно закрытой окислом. Потенциал электрода при этом самопроизвольно смещается в область высоких положительных значений ( 1 - 7 в) и наступает анодная пассивность. [23]
Возрастание Ьк при переходе от 50 к 25 С, по-видимому, обусловлено увеличением степени заполнения поверхности электрода хло-ридными комплексами нульвалентной платины, которые тормозят скорость электроосаждения платины. [24]
Эти данные, полученные из гальваностатических кривых спада потенциала, свидетельствуют о том, что степени заполнения поверхности электрода адсорбированными ингибиторами велики. [25]
 |
Скорость катодного оса - ли. щ ш. [26] |
Опыты, поставленные с полонием при его постоянной концентрации, показали постоянство скорости осаждения, что говорит о независимости последней величины от степени заполнения поверхности электрода осаждаемым элементом. [27]
Здесь Со и С ( - емкость двойного слоя в исходном растворе электролита и в том же электролите, но с добавкой ПАВ в концентрации, обеспечивающей его адсорбционное насыщение; Э - степень заполнения поверхности электрода ПАВ; fx - сдвиг потенциала нулевого заряда вследствие адсорбции. [28]
В результате электрохимического акта образуется адсорбированный катодом атомарный водород. Степень заполнения поверхности электрода адсорбированным атомарным водородом в условиях его катодного выделения определяется в первую очередь природой металла и для данного металла зависит от потенциала электрода. Она ничтожно мала ( 0 0) на Hg, Pb, Cd и на других мягких или ртутеподобных металлах. В согласии с этим выделение водорода по реакциям (17.78) и (17.79) может происходить несколькими путями и, соответственно, описываться различными кинетическими уравнениями. [29]
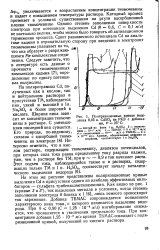 |
Поляризационные кривые выделения 0 05 н. CdSO. на РКЭ с добавками, t 25 С. [30] |
Страницы: 1 2 3