Степень - ионизация - кислота
Cтраница 1
Степень ионизации кислоты зависит также от стерических факторов. Обнаружено также, что величины Ка для ионизации первой группы дикарбоновой кислоты больше величин Ка для ионизации второй карбоксильной группы, если только эти группы не подвержены разным по характеру и величине влияниям. Различие в величинах первой и второй констант диссоциации отчасти связано со статистическими факторами, а отчасти со структурными. Первый из этих факторов заключается в том, что две СООН-группы имеют больше возможностей для взаимодействия с протоном, чем одна СООН-группа, а две С00 - - грушш более эффективно, чем одна С00 - - группа, захватывают обратно протон. [1]
По величине степени ионизации кислоты делятся на сильные и слабые. Поскольку сильные кислоты ионизированы полностью, растворы их имеют большую концентрацию ионов водорода. Поэтому рН раствора сильных кислот вычисляется с учетом пон. [2]
В зависимости от степени ионизации кислоты классифицируют следующим образом. [3]
В зависимости от степени ионизации кислоты можно разделить на сильные, которые легко ионизируются ( например, соляная, серная), слабые - ионизируются трудно ( например, уксусная, муравьиная) и кислоты промежуточной активности. [4]
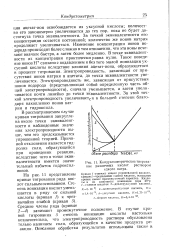 |
Кондуктометрическое титрование различных кислот раствором едкого натра. [5] |
В случае кривой титрования 5 степень ионизации кислоты настолько незначительна, что электропроводность раствора обусловлена только наличием соли, образующейся в качестве продукта реакции. [6]
При точных расчетах следует учитывать, что при разбавлении раствора несколько изменяется степень ионизации кислоты даже в присутствии ее соли. [7]
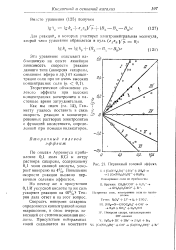 |
Первичный солевой аффект. [8] |
Скорость инверсии сахарозы определяется концентрацией ионов гидроксония, в свою очередь зависящей от степени ионизации кислоты. [9]
Фактически этот график аналогичен графику для случая ионизации слабой кислоты, и наклоны прямых здесь не зависят от степени ионизации кислоты. [10]
Ап - Н ], то при уменьшении рН раствора большее число ионов Н присоединяется к аниону An -, степень ионизации кислоты НАп в поверхностном слое понижается и заряд частичек уменьшается. Наступает, наконец, так называемая изоэлектрическая точка, когда заряд падает до нуля, и тогда происходит быстрая коагуляция коллоида. [11]
Такое использование констант кислотности для характеристики ионизации оснований было введено в 1923 г. Бренстедом, который увидел, насколько удобно выражать степень ионизации кислот и оснований в одной шкале, подобно тому, как значение рН одинаково хорошо характеризует и кислотность, и основность. Формальное сходство между процессами, описанными уравнениями (1.3) и (1.6), заключается в том, что в обоих случаях частицы, соответствующие написанным в знаменателе, при ионизации распадаются на протон и новое вещество, которое отличается по составу от исходного на ион водорода. [12]
Ап - I H ], то при уменьшении рН раствора большее число ионов Н присоединяется к аниону Ап -, степень ионизации кислоты НЛп в поверхностном слое понижается и заряд частичек уменьшается. Наступает, наконец, так называемая изоэлектрическая точка, когда заряд падает до нуля, и тогда происходит быстрая коагуляция коллоида. [13]
Ап - i H ], то при уменьшении рН раствора большее число ионов Ы присоединяется к аниону Ап -, степень ионизации кислоты НАп в поверхностном слое понижается и заряд частичек уменьшается. Наступает, наконец, так называемая изоэлектрическая точка, когда заряд падает до нуля, и тогда происходит быстрая коагуляция коллоида. [14]
К - я Ка - константы ионизации кислоты или основания - концентрационные ( Кс) и по активностям ( Ка); а - степень ионизации кислоты или основания ( см. стр. [15]
Страницы: 1 2