Степень - ионизация - электролит
Cтраница 2
Исходя из этого, теория сильных электролитов приписывает возрастание эквивалентной электропроводности с разбавлением раствора не увеличению степени ионизации электролита, а возрастанию скорости движения ионов вследствие разрежения ионной атмосферы и уменьшения межионных сил. [16]
Взяв отношение этих величин, находим а. Таким образом, формула Аррениуса дает практический метод определения степени ионизации электролита. [17]
Взяв отношение эти величин, находим а. Таким образом, формула Аррениуса дает практический метод определения степени ионизации электролита. [18]
В большинстве случаев q С с и Q 0: процесс диссоциации имеет эндотермический характер. Поэтому, в соответствии с принципом Ле Шателье, повышение температуры раствора приводит к увеличению степени ионизации электролита. [19]
Но между электродами все еще будет находиться 1 моль электролита, и величина Л будет фактически возрастать, так как в более разбавленных растворах движущиеся ионы испытывают меньшее задерживающее влияние других ионов и к тому же возрастает степень ионизации электролита. [20]
Активность и устойчивость ферментов сильно зависят от активности протонов в растворе. Немаловажное значение имеет и ионная сила раствора. В присутствии органических добавок и при понижении температуры степень ионизации электролитов уменьшается, что приводит к снижению растворимости и изменению активности протонов. [21]
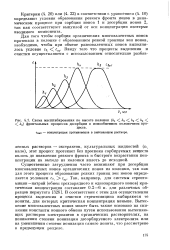 |
Схема масштабирования по высоте колонок ( fej h2 / i3 h4 C 5 фронтальных процессов десорбции в ионообменном колоночном процессе. свыт - концентрация противоионов в вытекающем растворе. [22] |
Существенные затруднения часто возникают при десорбции многовалентных ионов органических ионов из колонки, так как для этого процесса образование резких границ зон ионов определяется условием c0l скр. В соответствии с этим для осуществления процесса выделения и очистки стрептомицина выбираются те иониты, для которых критическая концентрация меньше. Вытеснение многовалентных ионов может быть также основано на снижении константы ионного обмена путем использования вытесняющих растворов электролитов в органических растворителях, на понижении степени ионизации десорбируемого электролита или на уменьшении степени ионизации самого ионита, что рассмотрено в предыдущем разделе. [23]
Страницы: 1 2