Степень - ассоциация
Cтраница 1
Степень ассоциации зависит от давления пара и уменьшается по мере дегидроксилирования поверхности. [1]
Степень ассоциации зависит от температуры, поскольку взаимодействие включает скорее образование легко диссоциирующих водородных связей [39], нежели образование ионных пар с формальным разделением заряда, причем стабилизация ионов путем их сольватации мала или вовсе отсутствует. На это указывает температурная зависимость теплоты нейтрализации олеиновой кислоты диметиламиноэтилметакри-латом ( табл. III. Хотя эти данные получены относительно простым калориметрическим методом [40 ] и их следует рассматривать только как приблизительные, они хорошо иллюстрируют общие тенденции. [2]
Степень ассоциации зависит от давления пара и уменьшается по мере дегидроксилирования поверхности. [3]
Степень ассоциации зависит от температуры. Доказано, что в жидкой воде при разных условиях устанавливается соответствующее динамическое равновесие между ассоциированными и неассоциированными молекулами. [4]
Степень ассоциации зависит также от кислотного остатка, входящего в состав соли, и температуры. [5]
Степень ассоциации можно найти путем определения числа t - тых ионов, находящихся на расстоянии, меньшем h, от данного / - того иона. [6]
Степень ассоциации является статистической величиной и определяется температурой; повышение температуры сдвигает кривую динамического равновесия в сторону преобладания индивидуальных молекул, понижение температуры - в сторону преобладания комплексов. [7]
Степень ассоциации зависит от длины кислотного остатка ( от числа атомов углерода в жирной кислоте), на тем меньше, чем длиннее этот остаток. С повышением температуры степень ассоциации уменьшается. Все особенности поведения углеводородных растворов солей жирных кислот в первом приближении хорошо объясняются электростатическим притяжением полярных молекул в яеполярном растворителе. [8]
Степень ассоциации таких соединений в значительной мере зависит от их концентрации в растворе и от алкильнои группы в ди-алкилалюминийфториде. [9]
Степень ассоциации является статистической величиной и определяется температурой; повышение температуры сдвигает кривую динамического равновесия в сторону преобладания индивидуальных молекул, понижение температуры - в сторону преобладания комплексов. [10]
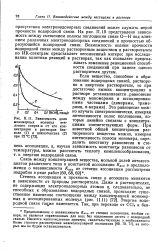 |
Зависимость доли мономерных молекул этилового спирта а от его концентрации в растворах бензола ( 1 и циклогексана ( 2 при 22 С. [11] |
Степень ассоциации и прочность связи в ассоциате меняются в зависимости от природы растворителя. Энергия водородной связи также изменяется. [12]
Степень ассоциации зависит также от кислотного остатка, входящего в состав соли, и температуры. [13]
 |
Взаимное положение по - дексов получило название ассоциа-лярных молекул в жидкости. ( объединение. К ассоцциро. [14] |
Степень ассоциации бывает различной. Сильно ассоциированные жидкости заметно отличаются от нормальных по многим свойствам. Ассоциация вызывает увеличение теплоты испарения, уменьшает летучесть жидкости и соответственно изменяет другие свойства. [15]
Страницы: 1 2 3 4