Степень - окисление - углерод
Cтраница 1
Степень окисления углерода в СО2 максимальная ( 4), а потому диоксид не может быть восстановителем, не горит, и не поддерживает горения. В его атмосфере горят простые вещества, атомы которых обладают большим сродством к кислороду, чем углерод. [1]
Степень окисления углерода зависит от кратности связи углерод-углерод в соединении. [2]
Какова степень окисления углерода в оксиде углерода ( IV) и изменяется ли она при образовании из углекислого газа угольной кислоты. [3]
Поэтому степень окисления углерода в изомерах не изменяется при переходе от одной структуры к другой. [4]
Укажите степени окисления углерода и марганца в составе реагентов и продуктов этой реакции. Ни одно из участвующих в реакции веществ не является пероксидом. [5]
Чему равны степени окисления углерода и брома до и после реакции. Какой элемент окисляется и какой восстанавливается. [6]
Как изменяется степень окисления углерода и хлора в этой реакции. [7]
Например, определим степени окисления углерода в различных соединениях. [8]
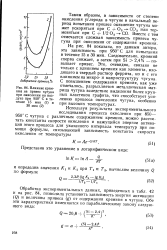 |
Влияние кремния на привес чугуна при окислении на воздухе при 950е1 С в течение 15 мин ( / и 30 мин ( 2. [9] |
Таким образом, в зависимости от степени окисления углерода в чугуне в начальный период испытания процесс окисления чугуна может ускоряться при С - f - O2 - - CO2 или тормозиться при С - f - 1 / 2 О2 - - СО. Вместе с тем отмечается сложная зависимость привеса чугуна при окислении от содержания кремния. На рис. 84 показана, по данным автора, эта зависимость при 950 С для испытания в течение 15 и 30 мин. Следовательно, кремний сперва снижает, а затем при Si 2 4 % - повышает привес. Это, очевидно, связано не только с влиянием кремния как элемента, входящего в твердый раствор феррита, но и с его влиянием на микро-и макроструктуру чугуна. С повышением содержания кремния, как уже отмечалось, разрыхляется металлическая матрица чугуна вследствие выделения более крупных пластинок графита, что способствует усилению процесса окисления чугуна, особенно при высоких температурах. [10]
В органической химии, как правило, степенями окисления углерода не оперируют, но если необходимо, то их оценивают по тем же правилам. При этом степень окисления углерода находят для каждого атома отдельно. [11]
В результате образуется формиат натрия, в котором степень окисления углерода 2, как и в оксиде. В этой реакции, равно как и вышеприведенной реакции получения СО из муравьиной кислоты, формально проявляется кислотная функция оксида углерода. [12]
Из других соединений углерода с неметаллами, где степень окисления углерода 4, следует отметить галогениды СНаЦ, сульфид CS2, оксо - и сульфогалогениды СОНаЬ и CSHab. Так ССЦ широко применяется в качестве негорючего растворителя органических веществ, а также жидкости для огнетушителей. [13]
В результате образуется формиат натрия, в котором степень окисления углерода 2, как и в оксиде. В этой реакции, равно как и в вышеприведенной реакции получения СО из муравьиной кислоты, формально проявляется кислотная функция оксида углерода. [14]
Процесс гликолиза включает два окислительно-восстановительных этапа, однако суммарного изменения степени окисления углерода в результате этого процесса не происходит. Легко видеть, что соотношение атомов С, Н и О в молекулах двух этих соединений одинаково и, следовательно, превращение глюкозы в молочную кислоту не сопровождается окислением углерода. Тем не менее при анаэробном гликолизе какая-то часть энергии, заключенной в молекуле глюкозы, все же извлекается; этой энергии достаточно для того, чтобы обеспечить суммарный выход двух молекул АТР в расчете на каждую расщепленную молекулу глюкозы. [15]
Страницы: 1 2 3 4