Степень - пассивность
Cтраница 1
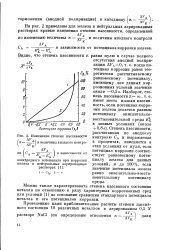 |
Изменение степени пассивности и величины анодного контро. [1] |
Степень пассивности, рассчитанная по анодному контролю Са и выражаемая в процентах, изменяется в этих условиях от нуля, если потенциал коррозии соответствует равновесному потенциалу железа для данных условий, и до 100 %, если значение потенциала железа равно окислительно-восстановительному потенциалу среды. [2]
Степень пассивности никелевых анодов растет с повышением анодной плотности тока DA, а также с понижением температуры раствора. [3]
Устойчивость этой степени пассивности анода зависит от величины анодной плотности тока, применяемой при длительном электролизе. [4]
Более точно степень пассивности металла при каждом потенциале может быть определена тангенсом угла касательной в данной точке анодной поляризационной кривой. [5]
Ряд возрастания степени пассивности, естественно, не будет прямо соответствовать ряду повышения коррозионной стойкости металлов в данных условиях. Это объясняется тем, что коррозионная стойкость зависит не только от пассивности ( анодного торможения), но и от катодного торможения, и термодинамической стабильности металла в данных условиях. Магний, наоборот, несмотря на высокую степень своей пассивности недостаточно стоек в указанных условиях. Однако если бы магний не имел достаточно высокой степени пассивности, он в данных условиях ( исходя из низкой его термодинамической стабильности) должен был бы корродировать в десятки раз быстрее. [6]
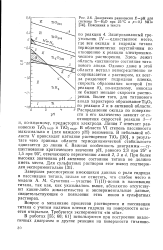 |
Диаграмма равновесия. рН для системы Ti - H2O при 25 С и / 50 1 МПа. Пояснения в тексте. [7] |
В области VI степень пассивности максимальна и ( для каждого рН) неизменна. При более высоких значениях рН активное состояние титана не должно иметь места. [8]
 |
Перенапряжение при выделении кислорода на различных металлах. [9] |
Очевидно, что в зависимости от степени пассивности анодной поверхности и характера образовавшихся на ней окислов может изменяться механизм разряда, а также величина перенапряжения выделения кислорода. Отсюда понятно, что предшествующая обработка анодной поверхности, а также продолжительность катодной или анодной поляризации электрода существенно влияют на процесс выделения кислорода. Сопоставляя зависимость перенапряжения кислорода и водорода от природы металла, можно заметить, что на металлах с низким перенапряжением водорода наблюдается высокое перенапряжение кислорода и, наоборот, на металлах с высоким перенапряжением водорода - перенапряжение кислорода мало. [10]
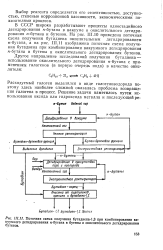 |
Поточная схема получения бутадиена-1 3 при комбинировании вакуумного дегидрирования н-бутана в бутены и окислительного дегидрирования. [11] |
Выбор реагента определяется его селективностью, доступностью, степенью коррозионной пассивности, экономическими показателями процесса. [12]
Определение пассивности, таким образом, позволяет количественно характеризовать степень пассивности металлов в различных коррозионных средах на основании известных величин потенциалов коррозии и начальных равновесных потенциалов анодного и катодного процессов. [13]
Ая ( рис. 121), величинз которого очевидно зависит от степени пассивности катода. Было установлено, что Ая зависит не только от загрязнения раство-ра, но и от длительности перерыв-а между двумя включениями тока. С увеличением перерыва Дя сначалз растет, а затем стабилизируется. Это нК - показывзет, что адсорбция совершается не мгновенно, а требует определенного времени. [14]
Таким образом, при одинаковом значении общего скачка потенциала ф меаду металлом и раствором степень пассивности различных участков металла может оказаться различной. Очевидно, при анодной активации металла в первую очередь будут депасеивиро-ваться те участки, на которых величина Аф имеет наименьшее значение. Таким образом возникает локализация процесса анодного растворения пассивного металла. На однородном металле этот эффект является статическим. [15]
Страницы: 1 2 3