Степень - покрытие - поверхность - катализатор
Cтраница 1
Степень покрытия поверхности катализатора изменяется с температурой, в результате чего температурная зависимость адсорбции, накладываясь на температурную зависимость скорости реакции, будет сказываться на величинах Е, получаемых на опыте. [1]
Значение а характеризует степень покрытия поверхности катализатора азотом в условиях процесса синтеза аммиака. [2]
Возможны промежуточные схемы, когда степень покрытия поверхности катализатора водородом зависит от строения гидрируемых соединений. [3]
Это фактически означало бы, что компенсационный эффект обусловлен изменением степени покрытия поверхности катализатора исходными веществами, как вытекает из смысла указанных уравнений, определяющих значения показателей степеней. [4]
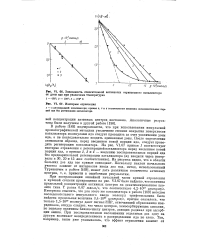 |
Зависимость относительной активности отравленного катализатора от дозы яда при различных температурах.| Изотермы отравления. [5] |
В работе [189] подчеркивается, что при использовании импульсной хроматографической методики увеличение степени покрытия поверхности катализатора молекулами яда следует проводить за счет увеличения дозы яда, а не последовательно вводить одинаковые дозы. После определения активности образца, перед введением новой порции яда, следует проводить регенерацию катализатора. Из рисунка видно, что в области больших доз яда все кривые совпадают. [6]
Это свидетельствует о том, что скорость реакции определяется взаимодействием спирта с поверхностным кислородом, причем степень покрытия поверхности катализатора кислородом близка к единице. В процессе этого взаимодействия, очевидно, и образуется указанный алкоголятный комплекс. [7]
 |
Гидрирование фенилпропио. [8] |
В данном случае мы имеем характерную для перехода от тройной к двойной связи картину - с ростом скорости реакции растет и степень покрытия поверхности катализатора водородом. При поглощении 53 % водорода раствор уже но содержит фенилацстилена. На платиновой черни гидрирование проходит при более высоком значении потенциала ( 990 и 1030 мв), что соответствует более прочной связи водорода с поверхностью. Исходное соединение в этом случае исчезает из раствора после поглощения 64 % водорода. [9]
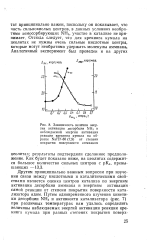 |
Зависимость величин энергии активации десорбции NH3 и наблюдаемой энергии активации реакции крекинга кумола на образце NaHF-80 ( 7 9 от степени покрытия поверхности аммиаком. [10] |
Другим принципиально важным вопросом при изучении связи между кислотными и каталитическими свойствами является оценка центров катализа по энергиям активации десорбции аммиака и энергиям активации самой реакции от степени покрытия поверхности катализатора ядом. [11]
При варьировании условий процесса совокупность стадий и промежуточных соединений может сохраняться неизменной, хотя изменится соотношение скоростей стадий ( например вследствие разной их температурной зависимости) или степень покрытия поверхности катализатора. Вопрос о соотношении скоростей стадий, строго говоря, в понятие механизма не входит, хотя его можно считать кинетической производной этого понятия. Разные соотношения скоростей стадий могут отвечать одному и тому же механизму, как и протекание реакции в разных областях заполнений поверхности катализатора. Это не исключает важность и необходимость выяснения соотношения скоростей стадий процесса в изучаемых условиях, что и является одной из задач исследования кинетических закономерностей. [12]
Для анализа закономерностей, указывающих на множественность стационарных режимов реакции гидрирования окиси углерода [279], как и для интерпретации возникновения автоколебаний в процессе окисления водорода на никеле [468], принимается зависимость энергии активации некоторых стадий от степени покрытия поверхности катализатора вследствие взаимного влияния в поверхностном слое. Такая зависимость также может быть описана обсуждаемыми линейными соотношениями энергии Гиббса. [13]
Таким образом, теория процессов на неоднородных поверхностях приводит к неожиданному результату: в области средних заполнений, если адсорбируется преимущественно один из компонентов реакции, при наличии соотношения линейности, кажущаяся энергия активации может не зависеть от того, на каких местах поверхности протекает реакция и какова максимальная адсорбционная способность катализатора. Следовательно, в таком случае изменение степени покрытия поверхности катализатора ( при сохранении области средних заполнений), выведение из сферы реакции некоторых участков благодаря отравлению их или спеканию, может не обязательно изменять величину кажущейся энергии активации. При этом, разумеется, истинная энергия активации должна, как правило, изменяться при переходе от одного места поверхности к другому. [14]
Рогинский учитывает взаимосвязь величин энергии активации реакции, изменения работы выхода электрона и степени покрытия поверхности катализатора. Так, если скорость процесса определяется скоростью адсорбции одно-го из веществ, то из уравнений (III.241), (III.242), (III.250) и (III.256) получаются уравнения кинетики с дробными степенями, обусловленными изменением работы выхода электрона в результате адсорбции. [15]
Страницы: 1 2