Степень - протолиз
Cтраница 1
Степень протолиза возрастает в ряду La111 - Lu 1; в том же Порядке упрочняется связь Ln - OH2 и, соответственно, ослабляется связь О - Н в координированной воде, что и повышает степень отрыва протона и переноса его к воде-растворителю. [1]
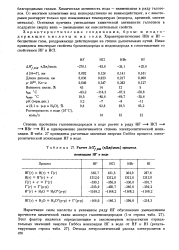 |
Расчет ДСу ( кДж / моль процесса ионизации НГ в воде. [2] |
Степень протолиза галогеноводородов в воде растет в ряду HF - HCI - - НВг - HI и одновременно увеличивается степень электролитической ионизации. В табл. 27 приведены расчетные значения энергии Гиббса процесса электролитической ионизации НГ в воде. [3]
Степень протолиза НСЮ в присутствии HNO3 уменьшается в 13 316 раз. [4]
 |
Расчет Д G298 ( кДж / моль процесса ионизации НГ в воде. [5] |
Степень протолиза галогеноводородов в воде растет в ряду HF - - НС1 - - HBr - - HI и одновременно увеличивается степень электролитической ионизации. В табл. 11 приведен расчет энергии Гиббса процесса электролитической ионизации НГ в воде. [6]
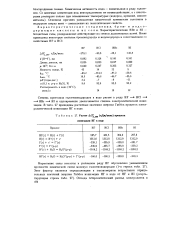 |
Расчет ДСу 2gg ( кДж / моль процесса ионизации НГ в воде. [7] |
Степень протолиза галогеноводородов в воде растет в ряду HF - НС1 - - НВг - HI и одновременно увеличивается степень электролитической ионизации. В табл. 27 приведены расчетные значения энергии Гиббса процесса электролитической ионизации НГ в воде. [8]
Если степень протолиза слабой кислоты НА в воде равна 0 27 %, а слабой кислоты НВ - 8 3 %, можно ли ( да, нет) утверждать, что кислота НВ сильнее кислоты НА. [9]
Расчет степени протолиза слабого протолита и ее уменьшение в присутствии избытка одноименных ионов среды проводится с применением этих соотношений. [10]
Очевидно, что степень протолиза аНА при разбавлении ( увеличении объема) раствора возрастает, а концентрация Н3О уменьшается. [11]
Усиливается или уменьшается степень протолиза аквакатионов с увеличением степени окисления металла, входящего в состав этого катиона. [12]
Объясните, почему полученные значения степени протолиза близки между собой. [13]
Обратите внимание, что в расчетную формулу для степени протолиза не входит концентрация слабой кислоты или слабого основания, если слабый протолит находится в присутствии избытка одноименных ионов среды протолиза. [14]
Кислоты и основания могут сильно отличаться друг от друга по степени протолиза в воде. Сильные протолиты почти нацело реагируют с растворителем. [15]
Страницы: 1 2