Степень - протонизация
Cтраница 1
Степень протонизации зависит от молекулярной массы и строения сульфида. [2]
Степень протонизации вещества в растворе кислоты с данной функцией кислотности Гаммета, как ясно из вышеизложенного, определяется основностью вещества, Для различных углеводородов, являющихся в общем очень слабыми основаниями, основность изменяется в очень широких пределах. [3]
Степень протонизации отщепляющегося водорода, по-видимому, значения не имеет. [4]
В степени протонизации важную роль играет стабилизация аниона. [5]
 |
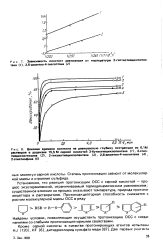
Частоты полос поглощения группы N-H в ИК-спектрах амидов RCONHR. [6] |
При R R СН3 степень протонизации водородного атома уменьшается вследствие проявления этими группами / - эффекта, что приводит к ослаблению водородной связи. Фенильная группа, характеризующаяся - / - и С-эффектами, оказывает противоположное действие при введении ее в амидную R или карбонильную R часть молекулы, увеличивая силу водородной связи в первом случае и уменьшая ее во втором. [7]
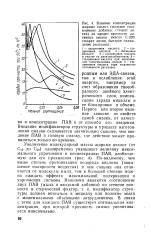 |
Влияние концентрации жирных кислот ( мольное соотношение добавка. стеарат лития на предел прочности литиевых смазок ( масло С-220, стеарат лития, быстрое охлаждение расплава. [8] |
По-видимому, чем выше степень протонизации водорода кислоты ( повышение полярности вещества) и чем сильнее она отличается от молекулы мыла, тем в большей степени можно ожидать эффекта максимальной поляризации и упрочнения системы. В связи с этим для каждого ПАВ существует оптимальная концентрация, при которой прочность смазки увеличивается максимально. [9]
Как уже было указано, подвижность трехуглеродной системы зависит от степени протонизации атома водорода; поэтому для различных ядерно-замещенных изомеров вышеуказанного типа подвижность тем больше, чем больше - / - и - С-эффекты имеющихся в ядре заместителей; это было подтверждено экспериментально. Положение же равновесия определяется относительной устойчивостью отдельных изомеров. [10]
Хаммет предположил, что простая концентрация Н дает возможность экспериментально измерять степень протонизации в разбавленных растворах, соответствующий член в уравнении (XVI.5.4) можно использовать для измерения этого свойства в концентрированных растворах. [11]
Рассмотрены условия образования полиметаллических комплексов и выявлены области их существования в зависимости от степени протонизации лиганда. [12]
Y должны влиять противоположным бразом - оттягивающие электроны увеличивать скорость процесса, следствие увеличения степени протонизации водорода в амино-руппе, а заместители, подающие электроны, - замедлять. Если же ерно второе предположение, следует ожидать, что скорость резкий, наоборот, должна увеличиваться при увеличении положитель-ой заряженности атома углерода карбоксильной группы и донорной пособности атома азота аминогруппы. [13]
Он отмечает, что при заданной силе акцептора протона сила водородной связи зависит от условий, определяющих степень протонизации водорода. Условием образования короткой водородной связи является фиксация электронного облака при оттягивании протона. Это положение иллюстрируется результатами измерений инфракрасных спектров. [14]
В спектрах протонного магнитного резонанса ассоциация посредством водородной связя вызывает обычно сдвиг сигнала в область слабых полей, что объясняется увеличением степени протонизации ( уменьшением степени экранирования) атома водорода. [15]
Страницы: 1 2 3