Степень - протонизация
Cтраница 2
Состояние равновесия, однако, определяется не только константой скорости енолизации, которая находится при прочих равных условиях в прямой связи со степенью протонизации водорода, но также и от константы скорости обратного процесса-скорости кето-низации енола. Последняя также зависит от наличия в соединениях различных замещающих групп. [16]
Состояние равновесия, однако, определяется не только константой скорости енолизации, которая находится при прочих равных условиях в прямой связи со степенью протонизации водорода, но также и от константы скорости обратного процесса-скорости кетонизации енола. Последняя также зависит от наличия в соединениях различных замещающих групп. Кроме того, важным фактором, влияющим на константу скорости кетонизации, является наличие внутримолекулярной водородной связи; енольные формы соединений, рассмотренных выше, как правило, содержат такую связь, что обусловливает уменьшение константы ионизации. [17]
Ассоциаты силанолов с эфирами и подобными соединениями, несомненно, образованы при участии атома водорода гидроксиль-ной группы силанола, и поэтому прочность их прямо зависит от степени протонизации силанола. Из данных табл. 12 следует, что силанолы являются существенно более сильными кислотами, чем аналогично построенные гидроксильные производные углерода, германия и олова. [18]
Если правильно первое предположение, то в бензоилхлориде заместители X, подающие электроны к углероду карбонильной группы, должны увеличивать скорость процесса, а оттягивающие-замедлять; в анилине же заместители Y должны влиять противоположным образом-оттягивающие электроны увеличивать скорость процесса, вследствие увеличения степени протонизации водорода в аминогруппе, а заместители, подающие электроны-замедлять. Если же верно второе предположение, следует ожидать, что скорость реакции, наоборот, должна увеличиваться при увеличении положительной заряженности атома углерода карбоксильной группы и донорной способности атома азота аминогруппы. [19]
Эти показатели дают основание думать, что водородные атомы гидроксильных групп нашего синтана слабо протонизованы из-за применения алкилированных слабокислых смоляных фенолов и сравнительно высокой степени сульфометилирования. От степени протонизации водородного атома в дубителе зависит прочность водородных связей, составляющих основу механизма дубления кожи. Относительно невысокий уровень кожевенно-тех-нологических свойств нашего дубителя объясняется также пониженным содержанием гидроксильных групп в дубителе, что обусловлено применением смоляных фенолов при синтезе. [20]
Он может быть использован в тех случаях, когда вблизи ы одной из форм ( например, А) поглощение второй формы либо слаб зависит от длины волны, либо близко к нулю. При наличии бокового сдвига одновременно с из менением степени протонизации будет наблюдаться постепенное сме щение Хмакс смеси, но поглощение при этом максимуме будет зависел только от степени протонизации. [21]
Так, меняя рН водной фазы, можно изменять степень протонизации солей органических кислот или переводить их в эфиры. При изменении формы неорганических соединений используют реакции комплексообра-зования. [22]
При замене СН3О - группы в ядре другими группировками подвижность и положение равновесия таких систем изменяются. Как уже было сказано, подвижность трехуглеродной системы зависит от степени протонизации атома водорода; поэтому для различных ядер но-замещенных изомеров вышеуказанного типа подвижность тем больше, чем больше - / - и - С-эффекты имеющихся в ядре заместителей; это было подтверждено экспериментально. Положение же равновесия определяется относительной устойчивостью отдельных изомеров. [23]
Он может быть использован в тех случаях, когда вблизи ы одной из форм ( например, А) поглощение второй формы либо слаб зависит от длины волны, либо близко к нулю. При наличии бокового сдвига одновременно с из менением степени протонизации будет наблюдаться постепенное сме щение Хмакс смеси, но поглощение при этом максимуме будет зависел только от степени протонизации. [24]
Поэтому в разбавленных водных растворах кислот, кислотность которых еще может быть количественно отражена рН - шкалой, основные свойства подавляющего большинства из них - спиртов, альдегидов и кетонов, простых и сложных эфиров и др., обнаруживаются только такими методами, которые достаточно чувствительны для регистрации очень маленьких степеней протонизации. Главным из таких методов является изучение кислотнокаталитических реакций оксониевых оснований ( см. гл. [25]
Смещение электронов от Н к А само по себе еще не означает, что в водородном мостике атом Н приобретает положительный заряд. В самом деле, вследствие донорно-акцепторного взаимодействия между атомами Н и В облако неподеленной пары электронов последнего несколько смещается в направлении к атому Н и частично или полностью нейтрализует его заряд. Вопрос о степени протонизации атома водорода в водородном мостике еще не выяснен. [26]
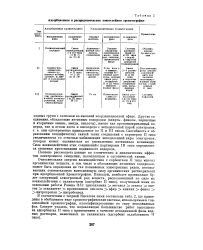 |
Адсорбционная и распределительная тонкослойная хроматография. [27] |
Способность к образованию специфических связей таких соединений с партнером II типа увеличивается со степенью мобилизации неподеленной пары электронов, которая может оцениваться по уменьшению потенциала ионизации. Сила взаимодействия этих соединений с партнерами III типа определяется степенью протонизации подвижного водорода. [28]
Определение основности растворов ароматических кетонов и ароматических карбоновых кислот в смесях серной кислоты с водой методом УФ-спектроскоции показало, что эти соединения являются более слабыми основаниями, чем анилин, приблизительно в 10 10 раз в в7 222 22з Такая же разница в основности наблюдается для растворов в серной кислоте полиаминов, с одной стороны, и дикето-нов, дикарбоновых кислот и кетокарбоновых кислот - с другой. При этом если две основные группы достаточно близки друг к другу, то дикетоны, дикарбоновые и кетокарбоновые кислоты в растворе серной кислоты присоединяют только один протон. С увеличением расстояния между двумя основными группами непрерывно увеличивается и степень протонизации. Максимальное значение v 3 0 в растворах дикарбоновых кислот не достигается; это еще не получило объяснения. [29]
Закономерное смещение характеристической частоты колебания связи в инфракрасном спектре наблюдается и в том случае, когда варьируют силу кислот, взаимодействующих с одним, и тем же основанием. По мере увеличения константы ионизации кислоты полоса смещается в направлении больших частот ( рис. 2Щ, В. М. Чулановский объясняет эту закономерность тем, что с ростом константы ионизации возрастает, как он выражается, степень обнаженности протона в водородном мостике. Иными словами, при взаимодействии молекулы кислоты АН с молекулой основания В электрон атома водорода входит в единую электронную оболочку с электронами атома А, которая сильнее связана с последним, чем с протоном. Образованию водородной связи сопутствует частичная протонизация атома водорода гидроксильной группы кислот, причем степень протонизации ( или обнаженности протона) тем больше, чем сильнее кислота. [30]
Страницы: 1 2 3