Степень - хроматографическое разделение
Cтраница 2
Сравнивают величины Vmax и константы обмена. Находят АУ для пары Са2 и Zn2 и делают вывод о степени хроматографического разделения. [16]
Сравнивают величины 1 / тах и константы обмена. Находят А У для пары Са2 и Zn2 и делают вывод о степени хроматографического разделения. [17]
Для характеристики разделительной способности колонки используют понятие удерживаемого объема: vg - t Fg, где tk - время выхода вещества; Fg - скорость газа-носителя; vg - удерживаемый объем газа-носителя, необходимый для проявления вещества и служащий константой для данного вещества. Удерживаемый объем или время выхода обычно используют для характеристики разделения компонентов анализируемой смеси. Степень хроматографического разделения различных газов на жидкости определяется величиной сил взаимодействия веществ с жидкой фазой. Из газовой смеси на разделительной колонке будет всегда сильнее удерживаться газ, лучше растворимый в жидкой фазе. [18]
Для характеристики разделительной способности колонки используют понятие удерживаемого объема: vg t Fg, где tu - время выхода вещества; Fg - скорость газа-носителя; vg - удерживаемый объем газа-носителя, необходимый для проявления вещества и служащий константой для данного вещества. Удерживаемый объем или время выхода обычно используют для характеристики разделения компонентов анализируемой смеси. Степень хроматографического разделения различных газов на жидкости определяется величиной сил взаимодействия веществ с жидкой фазой. Из газовой смеси на разделительной колонке будет всегда сильнее удерживаться газ, лучше растворимый в жидкой фазе. [19]
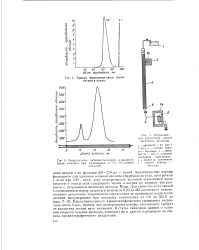 |
Кривые вымывания смеси ионов натрия и калия.| Распределение активности натрия и калия по. [20] |
Анализируемые порции фильтратом для удаления соляной кислоты упаривали до суха, прогревали в печи при 140, после чего оттптровывали щелочью оставшуюся часть кислоты и определяли содержание калия и натрия по хлориду ( по разности с титрованием щелочью) методом Мора. В статье приведены данные о влиянии скорости течения раствора, температуры и других параметров на степень хроматографического разделения. [21]
Для хроматографических аналитических опытов, выполняемых в небольших колонках и в практически равновесных условиях, оптимизация может быть ограничена обоснованным выбором статических факторов: природы и количества ионита, а также состава и концентрации промывающего раствора. Решение таких задач упрощается и отсутствием взаимного влияния компонентов в слое сорбента в ходе хроматографического опыта, поскольку на решающих стадиях развития хроматограмм движение компонентов с достаточной точностью может рассматриваться как независимое. В этих рамках и в представлении о применимости закона действующих масс к ионообменным процессам разработана простейшая теория, связывающая степень хроматографического разделения с перечисленными выше статическими факторами. В этом приближении степень хроматографического разделения характеризуется разностью объемов растворов AF, отвечающих максимумам выходных кривых компонентов разделяемой смеси. [22]
Для хроматографических аналитических опытов, выполняемых в небольших колонках и в практически равновесных условиях, оптимизация может быть ограничена обоснованным выбором статических факторов: природы и количества ионита, а также состава и концентрации промывающего раствора. Решение таких задач упрощается и отсутствием взаимного влияния компонентов в слое сорбента в ходе хроматографического опыта, поскольку на решающих стадиях развития хроматограмм движение компонентов с достаточной точностью может рассматриваться как независимое. В этих рамках и в представлении о применимости закона действующих масс к ионообменным процессам разработана простейшая теория, связывающая степень хроматографического разделения с перечисленными выше статическими факторами. В этом приближении степень хроматографического разделения характеризуется разностью объемов растворов AF, отвечающих максимумам выходных кривых компонентов разделяемой смеси. [23]
В ряде случаев использование комплоксообразующих реагентов влечет за собой своеобразие кинетических особенностей системы. Это связано с тем, что реакция комплексообразования, сопряженная с образованием неионных, координационных связей, не является бесконечно быстрой, а протекает с конечной скоростью. Особенно заметно это проявляется при наличии двух конкурирующих комплексных соединений в одной и той же системе, как это, например, происходит при разделении смесей редкоземельных элементов в присутствии ионов-замедлителей. В этом случае, по-видимому, скорость процесса в целом определяется скоростью реакции комплексообразования, вследствие чего степень хроматографического разделения не зависит от такого важного параметра опыта, как зернение сорбента. Все это ввиду существенного научного интереса и большого практического значения делает целесообразным детальное изучение кинетики хроматографических процессов в присутствии комплексообразующих реагентов. [24]
Страницы: 1 2