Степень - свобода - движение - молекула
Cтраница 1
Степени свободы движения молекул врашательная 216 ел. [1]
Эти 12 неприводимых представлений соответствуют 12 степеням свободы движения молекулы HNNH. [2]
Расчет теплоемкости многоатомных газов производится с учетом степеней свободы движения молекул. [3]
Известно, что энергия равномерно распределяется между степенями свободы движения молекулы. Числом 6 степеней свободы молекулы называют число координат, определяющих положение молекулы в пространстве. [4]
Известно, что энергия равномерно распределяется между степенями свободы движения молекулы. Числом етепеней свободы молекулы б называют число координат, определяющих положение молекулы в пространстве. [5]
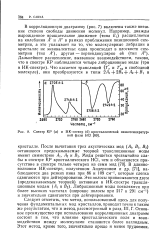 |
Спектр КР ( а и ИК-спектр ( б кристаллической низкотемпературной фазы НС1. [6] |
В корреляционную диаграмму ( рис. 7) включены также внешние степени свободы движения молекул. [7]
 |
Работа расширения газа. [8] |
Расчет теплоемкости многоатомных газов в кинетической теории производится с учетом степеней свободы движения молекул. [9]
Установленный Максвеллом - Больцманом закон о равнораспределении энергии утверждает, что на каждую степень свободы движения молекулы расходуется одинаковое количество энергии. [10]
Понятие о степени свободы в правиле фаз не следует смешивать с понятием о степенях свободы движения молекул ( стр. [11]
Напомним также, что величина, равная V2 kT, является энергией, приходящейся на одну степень свободы движения молекул и совершенно не зависит от конкретной природы частиц. [12]
Зная энергию сублимации г и энтропию конденсата и выбрав по возможности такую температуру, когда одни степени свободы движения молекул пара полностью возбуждены, а другие, напротив, возбуждены столь мало, что заметно не проявляются ( и когда вследствие этого отпадает по - - правочный член эйнштейновских функций от характеристических температур пара, определение которых требует специального исследования), по формуле (6.19) можно вычислить химическую постоянную вещества по одной точке температурной кривой давления насыщенного пара. [13]
Один из основных законов кинетической теории газов гласит, что внутренняя энергия газа распределяется равномерно между степенями свободы движения молекул. [14]
Таким образом, дифференциальная теплота адсорбции определяет суммарную энергию, необходимую для удаления адсорбированной молекулы из ее среднего вибрационного состояния, для отрыва от адсорбированных соседних молекул на неопределенное расстояние от поверхности и для увеличения числа степеней свободы движения молекул при переходе из адсорбированного состояния в объемную газовую фазу. Отсюда следует, что величина адсорбционного потенциала практически эквивалентна дифференциальной мольной теплоте адсорбции. [15]
Страницы: 1 2