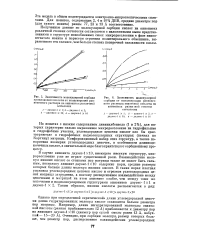
Степень - поперечная связанность
Cтраница 2
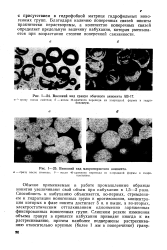 |
Внешний вид гранул обычного анионита АВ-17.| Внешний вид макропористого анионита. [16] |
Благодаря наличию поперечных связей иониты практически нерастворимы, а количество поперечных связей определяет предельную величину набухания, которая уменьшается при возрастании степени поперечной связанности. [17]
Каркас смолы обладает неправильной периодической структурой, обусловленной наличием беспорядочно расположенных поперечных связей, размеры пор в таком иопите неодинаковы и зависят от степени поперечной связанности. С увеличением степени поперечной связанности размеры пор уменьшаются, ячейки матрицы становятся недосягаемыми для больших комплексных и органических проткво-ионов. [18]
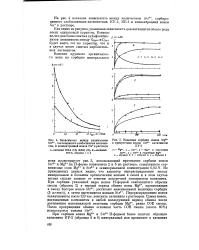 |
Зависимость между количеством [ IMAGE ] Кинетика сорбции ионов Mga Strs, поглощенного слабосшитым катиони - в присутствии ионов Str3 катионитом том, и концентрацией ионов Na в растворе ИУ-2. [19] |
Из приведенных данных видно, что характер перераспределения между минеральным и большим органическим ионами в смоле и в этом случае весьма сильно зависит от степени поперечной связанности катионита. Перераспределение ионов заканчивается после 120 час. Сумма ионов, поглощенных катионитом в любой последующий период обмена после достижения максимальной величины сорбции Mg2 1, равна СОЕ смолы. [20]
По величине обменной емкости в расчете на обезвоженное вещество макропористые и гелевые катиониты сходны между собой, но простая связь между коэффициентом влагоемкости и степенью поперечной связанности для них не выполняется. [21]
Полученные данные по молекулярной сорбции кислот на анионитах различной степени сетчатости согласуются с изложенными выше представлениями о структуре ионообменных смол: микрорасслоении в фазе низкосетчатого ионита и пористом строении полистирольного обменника, выраженного тем сильнее, чем больше степень поперечной связанности смолы. [23]
Повышение степени поперечной связанности влечет за собой понижение набухания смол в большей части растворителей, подобно тому, как это имеет место в случае воды. Изменения набухания в зависимости от состава раствора являются серьезной помехой при использовании смешанных растворителей в аналитической практике, так как они могут вызвать образование каналов в слое ионита или даже закупоривание колонки. Чтобы предотвратить подобные неполадки, колонку следует предварительно обрабатывать неводным или смешанным растворителем, который будет применяться в процессе работы. С другой стороны, рассматриваемый эффект может быть использован для анализа смешанных растворителей. Калмон [9 ] предложил применять для этой цели сульфированные иониты с низкой степенью поперечной связанности, например полистироловые смолы, содержащие менее 1 % дивинилбензола. Для калибровки строится кривая зависимости набухания от равновесного состава жидкой фазы. Метод проверен на метиловом, этиловом и пропиловом спиртах, ацетоне, диоксане и глицерине. [24]
Определенное влияние на обмен ионов оказывает структура матрицы ионита. Чем больше степень поперечной связанности, полимерной основы ионитов, тем слабее набухают они в воде и тем слабее выражена их способность к поглощению крупных, ионов. Иониты, обладающие наиболее упорядоченной структурой, называются изопористыми. [25]
Определенное влияние на обмен ионов оказывает структура матрицы ионита. Чем больше степень поперечной связанности полимерной основы ионитов, тем слабее набухают они в воде и тем слабее выражена их способность к поглощению крупных ионов. Иониты, обладающие наиболее упорядоченной структурой, называются изопористыми. [26]
Каркас смолы обладает неправильной периодической структурой, обусловленной наличием беспорядочно расположенных поперечных связей, размеры пор в таком иопите неодинаковы и зависят от степени поперечной связанности. С увеличением степени поперечной связанности размеры пор уменьшаются, ячейки матрицы становятся недосягаемыми для больших комплексных и органических проткво-ионов. [27]
Следует иметь л виду, что D нонит при набухании проникает ire только растворитель, по и электролит. С повышением степени поперечной связанности проникновение эл ектр и л и та у мсп ы п а стся. [28]
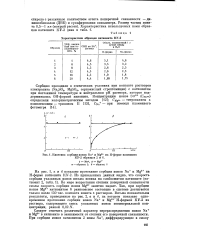 |
Кинетика сорбции ионов Na и Mga на Н - форме катионита КУ-2 образцов 2 и 6. [29] |
На рис. I, а и б показано протекание сорбции ионов Na и Mg2 1 на Н - форме катионита КУ-2. По мере возрастания степени поперечной связанности смолы скорость сорбции ионов Mg2 1 заметно падает. Так, при сорбции ионов Mg2 1 катионитом 6 равновесное состояние в системе достигается только после 150 час. [30]
Страницы: 1 2 3 4