Устойчивая степень - окисление
Cтраница 3
 |
Атомные радиусы бария, лантаноидов и гафния.| Ионные радиусы ( для координационного числа 6 Sc3, Y3, Ln3. [31] |
Все актиноиды, за исключением протактиния и, возможно, тория, имеют степень окисления ( III), но это не самая устойчивая степень окисления для некоторых из них. [32]
Вален гньш элсктрочрмй уровень атомов этих элементов отвечает формуле ns2np4 Кислород - второй по электроотрицательности элемент ( после наиболее отрицательного фтора), ему можно приписать устойчивую степень окисления в соединениях, равную ( - II); во фторидах кислорода его степень окисления положительна. [33]
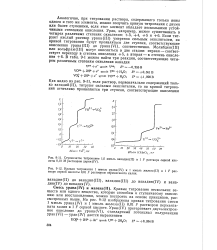
Аналогично, при титровании раствора, содержащего только ионы одного и того же элемента, можно получить кривую титрования с двумя или более ступенями, если этот элемент обладает несколькими устойчивыми степенями окисления. Если титруют кислый раствор урана ( III) умеренно сильным окислителем, на кривой титрования будут проявляться две ступени, соответствующие окислению урана ( III) до урана ( VI), соответственно. [35]
При описании окислительно-восстановительной способности элементов следует иметь в виду, что элемент, находящийся в степени окисления, которая ниже его устойчивой степени окисления, будет предпочтительнее проявлять восстановительные свойства, теряя электроны и стремясь перейти в устойчивую степень окисления. Элемент же, проявляющий степень окисления, которая выше его устойчивой степени окисления, будет проявлять окислительные свойства, при; нимая электроны и понижая свою степень окисления. Поэтому соединения марганца ( П) и ( III) являются преимущественно восстановителями, а соединения марганца ( У1) и особенно ( VII) - окислителями. [36]
Некоторые первые сведения о химии нептуния, полученные на индикаторных количествах этого изотопа, должны быть пересмотрены, так как в процессе работы с макроскопическими количествами вещества установлено, что нептуний обладает четырьмя ( а не двумя) устойчивыми степенями окисления. [37]
Групповое название этих элементов - халькогены, хотя кислород часто рассматривают отдельно. Его устойчивая степень окисления - П; положительная степень окисления у кислорода проявляется только в его соединениях с фтором. [38]
Для всех этих элементов возможно проявление нескольких степеней окисления: от 11 до VIII. Значение устойчивой степени окисления увеличивается сверху вниз по группе: например, III для Fe, IV для Ru, VIII для Os. Значение устойчивой степени окисления понижается слева направо в каждой триаде: например, III для Fe, 11 и III для Со, 11 для Ni. В свободном состоянии элементы УШБ-группы - тугоплавкие, белые с сероватым ( Fe, Co) или голубоватым ( Os) отливом. [39]
Кроме того, устойчивы степени окисления 2 всех Зй-металлов, начиная с Мп2 и до Zn2 включительно, а также степени окисления 3 для Sc, Cr, Fe. Таблица 23.3 показывает, что устойчивые степени окисления 3 -металлов образуют две группы: высшие ( 4, 5, 6, 7) и низшие ( 2, 3) степени окисления. [40]
 |
Отрицательный дифференц-эффект. [41] |
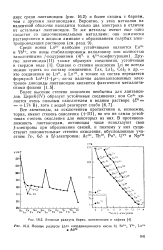
Наконец, в некоторых системах причиной отрицательного дифференц-эффекта служит образование при растворении металла ионов промежуточной степени окисления. Переход этих ионов в состояние устойчивой степени окисления осуществляется далее за счет химического взаимодействия с ионами Н или с молекулами Н2О с выделением водорода. [42]
Поэтому для ряда элементов побочных подгрупп устойчивые степени окисления следует просто запомнить. [43]
Поэтому для ряда, элементов побочных подгрупп устойчивые степени окисления следует просто запомнить. [44]
До сих пор, чтобы как можно меньше усложнять картину, обсуждение ограничивалось процессами, в которых от восстановителя к окислителю переносился один электрон. Большинство рассматриваемых примеров затрагивало комплексы переходных металлов, устойчивые степени окисления которых отличаются на единицу. Поэтому закономерен вопрос: может ли за один акт окисления-восстановления переноситься больше одного электрона. Если реакция идет по внешнесферному механизму, ограничение Франка-Кондона ( соответствие энергий окислителя и восстановителя до переноса электронов) будет намного более серьезным, когда дело касается переноса двух электронов; и более высокие значения энергий активации и меньшая вероятность успешного окислительно-восстановительного столкновения приведут к тому, что процесс этот станет маловероятным. Если реакция идет в растворе, ограничения могут быть, по-видимому, смягчены по той причине, что реагенты могут находиться в тесном соприкосновении друг с другом ( в сольватационной ловушке) достаточно долго, для того чтобы участвовать в двух последовательных актах переноса электронов. Если реагирующие промежуточные соединения не живут столь долгое время, чтобы их можно было обнаружить, этот тип процесса, вероятно, нельзя будет по-настоящему отличить от синхронного переноса двух электронов. В реакции, протекающей по внутрисферному механизму, мостиковая связь может сохраняться достаточно долго, и поэтому возможен последовательный перенос более чем одного электрона. [45]
Страницы: 1 2 3 4