Высшая степень - окисление - элемент
Cтраница 1
Высшая степень окисления элементов обычно отвечает номеру группы, причем в высших оксидах и гидрокси-дах кислотный характер растет слева направо по периодам, а основной - ослабевает. [1]
 |
Полярограмма смесей растворов солей кадмия, цинка и марганца.| Полярограмма ступенчатого восстановления хромата. [2] |
Высшая степень окисления элемента образует волну при более положительном потенциале, чем средняя ( или низшая) степень окисления. Это явление иногда используют для устранения влияния посторонних ионов. Так, двухвалентный никель восстанавливается легче двухвалентного кобальта и мешает определению последнего. [3]
Высшую степень окисления элемента определяет номер группы периодической системы, в которой он находится. [4]
 |
Спектр поглощения хромата ( VI калия ( / и дихромата ( VI калия ( 2. [5] |
Какие лиганды стабилизируют высшие степени окисления элементов. [6]
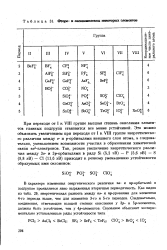 |
Фторо - и оксокошшексы некоторых элементов. [7] |
При переходе от I к VIII группе высшая степень окисления элементов главных подгрупп становится все менее устойчивой. [8]
При переходе от 1 к VIII группе высшая степень окисления элементов главных подгрупп становится все менее устойчивой. [9]
Подобное явление вообще характерно для производных, отвечающих высшим степеням окисления элемента. Например, соединение SCle не существует, a SO2C12 ( хлористый сульфурил) вполне устойчив. Оксогалогенидные производные типа ЭО3Г особенно характерны для технеция и рения. Все они представляют собой молекулярные соединения, строение которых однотипно. Так, молекула MnO3F представляет собой искаженный тетраэдр с атомом Мп в центре. [10]
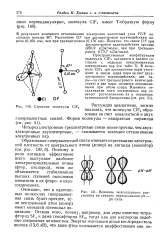 |
Строение молекулы C1F3.| Влияние межъядерного расстояния на степень перекрывания рл - рл-типа. [11] |
Поэтому в роли лигандов эффективнее всего выступают наиболее электроотрицательные атомы ( фтор, кислород), этим же объясняется стабилизация высших степеней окисления элементов в их фторо - и оксо-соединениях. [12]
 |
Некоторые свойства марганца, технеция, рения. [13] |
Для элементов подгруппы УНБ, как и других побочных подгрупп, при переходе от Мп к Re увеличивается устойчивость соединений с высшей степенью окисления элементов и усиливается тенденция к образованию кислотных оксидов и кислот. Так, Мп2О7 взрывается от малейшего Прикосновения, a Re2O7 образуется при нагревании рения на воздухе; НМпО4 является очень сильным окислителем, a HReO4 - слабый окислитель. [14]
 |
Некоторые свойства марганца, технеция, рения. [15] |
Страницы: 1 2 3