Высокая степень - стереоспецифичность
Cтраница 1
Высокая степень стереоспецифичности указывает либо на синхронную реакцию, либо на процесс, включающий две дискретных стадии образования связи, в котором вторая стадия проходит значительно быстрее, чем вращение вокруг уклсрод-углерадной связи в интермедиате. Наиболее широко распространена точка зрения, что большинство данных лучше согласуется с синхронной реакцией, модифицированной в некоторых случаях с тем, чтобы отразить различную степень образования связи с двух сторон. [1]
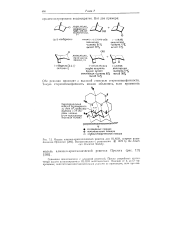 |
Модель алмазно-кристаллической решетки для HLADH, впервые разработанная Прологом. Воспроизведено с разрешения. 1978 by the American Chemical Society. [2] |
Обе реакции проходят с высокой степенью стереоспецифичности. [3]
Литийалкилы используются в качестве промоторов с высокой степенью стереоспецифичности при получении кристаллических высокомолекулярных полиолефинов. [4]
 |
Стереохимия реакций замещения в плоском квадратном комплексе с образованием тригонально бипирамидального интермедиата. Ассоциативное замещение с цыс-атакой и с сохранением конфигурации. [5] |
Полное сохранение конфигурации предполагает процесс с высокой степенью стереоспецифичности. Это очень мало вероятно для диссоциативного механизма, так как трикоординирован-ный интермедиат может иногда иметь приблизительно правильную ( с углами в 120) плоскую структуру. Затем в зависимости от того, войдет ли Y BPtA2L рядом с L или в положение напротив L, продукт PtA2LY может быть соответственно либо цис -, либо торакс-изомером. [6]
Полученные результаты ( см. формулы) говорят о высокой степени стереоспецифичности в смысле преобладания мс-элиминирования и указывают на согласованный механизм с переходным состоянием приведенного ниже типа. [7]
Лидс, Фукушима и Галлахер110 разработали общий метод синтеза стероидных гликолей, содержащих гидроксильные группы в кольце D, отличающийся хорошими выходами и высокой степенью стереоспецифичности. Процесс заключается в окислении енолацетатов 17-кетостериодов надбензойной кислотой, приводящем к соответствующим 17-ацетокси - 16а 17сс - окисям, которые затем восстанавливаются алюмогидридом лития в 16а 17 3-гликоли. Этот метод был использован для синтеза эстриола из эстрона. [8]
Напротив, цис - l, 2-дибромциклогексан не реагирует, так как лишь один из атомов брома может занять аксиальное положение. Высокая степень стереоспецифичности обнаруживается также при аналогичном дегалогенировании стереоизомерных 2 3-дибромбутанов. [9]
ЭУ реализуются механизмы 1 4 - и 1 3-дегидратации. Первый из них обладает высокой степенью стереоспецифичности и реализуется при цыс-1 4 - Н / ОН-расположении. Для 1 3-элиминирования молекулы воды у незамещенного циклогексанола стереоспеци-фичность не наблюдается, поскольку М 1, очевидно, имеет не циклическую структуру. [10]
Тщетно искать в этом случае молекулу циклопентанопергидрофе-нантрена. Приведенные выше реакции обладают высокой степенью стереоспецифичности, катализаторами для них служат ферменты и превращение идет строго направленно - образуется ряд определенных стереоизомеров, отбираемых среди тысяч возможных в столь сложных системах, как эта. Это и есть чудо природного органического синтеза. [11]
Возникает вопрос, реагируют ли производные кремния по механизму такого же типа. Исследования в области кинетики и стереохимии Зм-реакций при атоме кремния показали, что положение здесь значительно сложнее, чем при 8 2-реакциях алкилпроизводных. Так, хотя реакции SN-ТИПЗ при атоме кремния могут происходить с высокой степенью стереоспецифичности, их результатом может быть как обращение, так и сохранение конфигурации в зависимости от природы исходного соединения и характера уходящей группы. [12]
При этом, как можно видеть из рис. 17 - 11, меченая карбоксильная группа будет направлена в сторону руки фермента, тогда как немеченый карбоксил будет направлен в свободное пространство. Таким образом, две группы - СЩСОгН, химически эквивалентные в лимонной кислоте, становятся неэквивалентными при их сочетании описанным выше образом с асимметрическим ферментом. Можно ожидать, что в результате этого синтез а-кетоглутаровой кислоты должен происходить с высокой степенью стереоспецифичности. [14]
Страницы: 1 2

