Высокая степень - стереоспецифичность
Cтраница 2
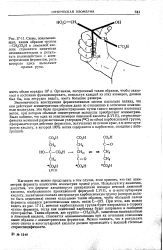
При этом, как можно видеть из рис. 17 - 11, меченая карбоксильная группа будет направлена в сторону руки фермента, тогда как немеченый карбоксил будет направлен в свободное пространство. Таким образом, две группы - СН2С02Н, химически эквивалентные в лимонной кислоте, становятся неэквивалентными при их сочетании описанным выше образом с асимметрическим ферментом. Можно ожидать, что в результате этого синтез а-кетоглутаровой кислоты должен происходить с высокой степенью стереоспецифичности. [16]
Напротив, перегруппировка по типу 5лг2 - замещения способствует стереохимически направленному протеканию реакции. При 1у2 - реакциях мигрирующая группа атакует неискаженный, тетраэдрический заряженный атом углерода. Следствием определенной ориентации реакционных центров является фиксированное положение входящего ( мигрирующего) заместителя, а отсюда - высокая степень стереоспецифичности замещения. В этом случае уже невозможно существование двух, разделенных энергетическим барьером ионов, как это имеет место в реакциях типа Sjyl, а существует лишь один неклассический ион, пространственная конфигурация которого строго фиксирована. [17]
Возникает вопрос, реагируют ли производные кремния по механизму такого же типа. Исследования в области кинетики и стереохимии SN-реакций при атоме кремния показали, что положение здесь значительно сложнее, чем при 8 2-реакциях алкилпроизводных. Стереохимические результаты не во всех случаях соответствуют представлению об обычном вальденовском обращении, сопровождающем Зм2 - механизм. Так, хотя реакции Sfj-типа при атоме кремния могут происходить с высокой степенью стереоспецифичности, их результатом может быть как обращение, так и сохранение конфигурации в зависимости от природы исходного соединения и характера уходящей группы. [18]
Наглядно это можно представить в том случае, если принять, что тип асимметрии фермента аналогичен асимметрии правой руки. Используя эту аналогию, допустим, что. При этом, как можно видеть из рис. 17 - 11, меченая карбоксильная группа будет направлена в сторону руки фермента, тогда как немеченый карбоксил будет направлен в свободное пространство. Таким образом, две группы - СН2СО2Н, химически эквивалентные в лимонной кислоте, становятся неэквивалентными, при их сочетании описанным выше образом с асимметрическим ферментом. Можно ожидать, что в результате этого синтез а-кетоглутаровой кислоты должен происходить с высокой степенью стереоспецифичности. [20]
Страницы: 1 2