Высшая положительная степень - окисление
Cтраница 1
Высшая положительная степень окисления проявляется, когда в образовании связи принимают участие все валентные электроны атома. Численно она равна номеру группы периодической системы и является важной количественной характеристикой элемента в его соединениях. Наименьшее значение степени окисления элемента, которое встречается в его соединениях, принято называть низшей степенью окисления. Все остальные степени окисления элемента называют промежуточными. [1]
Высшие положительные степени окисления - увеличиваются. Значение максимальной по величине отрицательной степени окисления для неметаллов уменьшается. [2]
Высшая положительная степень окисления проявляется, когда в образовании связи принимают участие все валентные электроны атома. Численно она равна номеру группы периодической системы и является важной количественной характеристикой элемента в его соединениях. Наименьшее значение степени окисления элемента, которое встречается в его соединениях, принято называть низшей степенью окисления. [3]
Высшая положительная степень окисления проявляется, когда в образовании связи принимают участие все валентные электроны атома. Численно она равна номеру группы периодической системы и является важной количественной характеристикой элемента в его соединениях. Наименьшее значение степени окисления элемента, которое встречается в его соединениях, принято называть низшей степенью окисления. Все остальные степени окисления элемента называют промежуточными. [4]
Высшая положительная степень окисления проявляется, когда в образовании связи принимают участие все валентные электроны атома. Численно она равна номеру группы периодической системы и является важной количественной характеристикой элемента в его соединениях. Наименьшее значение степени окисления элемента, которое встречается в его соединениях, принято называть низшей степенью окисления. Все остальные степени окисления элемента называют средними или промежуточными. [5]
Высшая положительная степень окисления проявляется, когда в образовании связи принимают участие все валентные электроны атома. Численно она равна номеру группы периодической системы и является с ж ной количеств е иной характеристикой: i мента в его соединениях. [6]
Высшая положительная степень окисления проявляется, когда в образовании связи принимают участие все валентные электроны атома. Численно она равна номеру группы периодической системы и является важной количественной характеристикой элемента в его соединениях. Наименьшее значение степени окисления элемента, которое встречается в его соединениях, принято называть низшей степенью окисления. Все остальные степени окисления элемента называют промежуточными. [7]
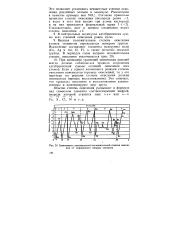 |
Зависимость максимальной положительной степени окисления от порядкового номера элемента. [8] |
Высшая положительная степень окисления атомов элементов определяется номером группы. [9]
Значение высшей положительной степени окисления не изменяется и равняется номеру группы. Значение максимальной по величине отрицательной степени окисления для неметаллов одинаково и равно 8 минус номер группы. [10]
Сера в соединении с фтором проявляет высшую положительную степень окисления. [11]
Сера в соединении со фтором проявляет высшую положительную степень окисления. [12]
В соединениях с кислородом элементы могут проявлять высшую положительную степень окисления, равную номеру группы. Оксиды элементов в зависимости от их положения в периодической системе и от степени окисления элемента могут проявлять основные или кислотные свойства. [13]
Оксид и глдроксид серы ( VI) имеют высшую положительную степень окисления, обладают сильными окислительными свойствами. [14]
Большинство остальных элементов имеют переменную степень окисления и, как правило, высшая положительная степень окисления численно равна номеру группы в периодической системе. [15]
Страницы: 1 2 3