Степухович
Cтраница 1
Степухович и другие [63] изучали влияние химической структуры растворителя на кинетику и механизм реакций Меншут-кина. [1]
Степухович и Митенков, Журн. [2]
Степухович [42] нашел, что скорость предельно заторможенной реакции крекинга этана с применением в качестве ингибиторов ацетилена, аллена и изобутилена существенно зависит от природы ингибитора. [3]
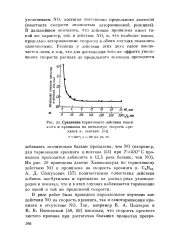 |
Сравнение тормозящего действия окиси азота и пропилена на начальную скорость крекинга н. пентана. [4] |
Степухович [57] количественно сопоставил действия добавок мзо-бутилена и пропилена на распад ряда углеводородов и показал, что и в этих случаях наблюдается торможение до одной и той же предельной скорости. [5]
По Степуховичу, скорость предельно заторможенной реакции зависит от природы ингибитора. [6]
Зыковой, Степуховича и др. [370, 371] по крекингу пентанов, заторможенных добавками пропилена и изобутилена. [7]
Итог многолетней работы Степуховича и Улицкого по изучению скорости и равновесия радикальных реакций опубликован в монографии [20] и других работах. Конечно, более десяти лет назад, когда готовилась эта монография, сведения о радикальных реакциях различных типов были весьма ограниченными. К настоящему времени значительно увеличилось число надежных данных о скоростях, механизме радикальных реакций, геометрических, механических и термохимических свойствах радикалов и других частиц. Известные трудности расчетов ab init о стимулируют более активное использование экспериментального материала для создания полуэмпирических методов в кинетике. [8]
Для выяснения того, насколько приемлемо приближенное уравнение Нернста, Степухович [281] на основе достаточно строгих термодинамических, статистических и кинетических соотношений рассчитал равновесия в реакциях присоединения и замещения атомов Н и - СН3 - радикалов с предельными и непредельными углеводородами и получил согласующиеся результаты. При высоких температурах в реакциях присоединения атомов Н к непредельным углеводородам ( С3Н6, зо - С4Н8, С2Н2, С3Н4) равновесие смещено в сторону образования сложных радикалов, что доказывает устойчивость этих радикалов к распаду. В тех же условиях равновесие реакций распада пропильных и бутильных радикалов на молекулы олефинов и - СН3 - радикалы сильно смещено в сторону образования продуктов распада, что свидетельствует о неустойчивости исходных радикалов. [9]
 |
Реакции присоединения HJ к молекулам олефинов. [10] |
Для реакций атома Н с этиленом, пропиленом и изобутиленом Степуховичем с сотрудниками были получены значения величины Р, которые приводятся в табл. 16, вместе с экспериментальными значениями. [11]
Ипатьев [1], Лебедев и Коблянский [2], Маккинли ( McKinley) с сотрудниками [3], [4], Краузе, Немцов и Соскина [5], [6], Флори ( Flory) [7], Степухович и Митенков [8] полимеризовали изобутилен с помощью теплоты и давления. [12]
 |
Термодинамические функции групп, составляющих алкильные радикалы, по Бенсону. [13] |
По термодинамическим функциям нетрудно рассчитать теплоты и константы равновесия с участием радикалов. Как отмечают Степухович и Улицкий, выполнившие расчеты К Р для ряда радикальных реакций 63 ], такие реакции протекают практически нацело, если АЯ - 60 кДж / моль и не протекает. [14]
Wiley, New York, 1973; Степухович, Бабаян. [15]
Страницы: 1 2