Изменение - перенапряжение
Cтраница 2
В качестве первого приближения можно принять, что изменение перенапряжения Ат ], вызванное изменением Афг, равно для нейтральных веществ Дф2 [ уравнение ( 2) гл. В этих случаях полезно отдельно изучать изменение скорости предшествующей реакции протонизации и влияние структуры двойного слоя. Скорость реакции протонизации определяется буферной емкостью, но структура двойного слоя остается неизменной, если поддерживать общую ионную силу постоянной. Влияние двойного слоя изучают, изменяя ионную силу [2]) при постоянной буферной емкости. Этот метод иллюстрируется рис. 159, на котором спад тока при больших отрицательных потенциалах вызван десорбцией восстанавливающегося вещества. Этот спад тем слабее выражен, чем больше скорость реакции протонизации. [16]
Ряд экспериментальных данных ( установление потенциала коррозии, изменение перенапряжения выделения водорода в гальвяно-статических условиях) подтверждает вывод о селективном растворении титана и о накоплении катодного компонента на поверхности сплава. Для некоторых композиций сплавов на основе исследования кинетики накопления на поверхности более электроположительного элемента, рассчитана площадь поверхности сплава, занятая этим легирующим компонентом. [17]
Хотя омическое падение потенциала в глубине раствора значительно влияет на изменение полного перенапряжения вдоль поверхности электрода, миграция в диффузионном слое не оказывает решающего влияния на распределение тока. В случае предельного тока мы видели, что роль миграции сводится к изменению величины тока, но не его распределения. [18]
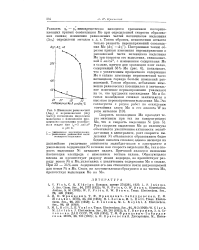 |
Изменение равноиесной ( Др0 и неравновесной ( Д ] частей потенциала выделения молибдена с изменением процентного содержания молибдена в осадке при il 5 ма. смг н рН 8. [19] |
Мо ( Д - г / - Дт ]) - Построенная таким образом кривая изменения перенапряжения и равновесной части потенциала выделения Мо при скорости его выделения, эквивалентной 5 ма / см, с изменением содержания Мо в сылаве, причем для сравнения взят сплав, содержащий 33 % Мо ( рис. 6), показывает, что с увеличением процентного содержания Мо в сплаве изменение неравновесной части потенциала гораздо больше изменений равновесной. [20]
Причем она зависит не только от стационарного потенциала чистых добавок и их коррозионной стойкости, а также от изменения перенапряжения на этих катодных добавках под влиянием насыщения их водородом. [21]
Экспериментальные данные показали, что в области потенциалов, в которой возможна адсорбция поверхностно-активных веществ на поверхности ртути, действительно наблюдается изменение перенапряжения выделения водорода. Сопоставление значений изменения перенапряжения в результате введения добавок с величиной адсорбционного пстенциала ( j) показало, что имеет место полуколичественное совпадение теории с результатами измерений. Это обстоятельство объясняется частичной десорбцией вещества с поверхности электрода при определенных значениях потенциалов. Молекулярные же добавки действуют слабее в результате того, что молекула в этом случае не создает вокруг себя поля, а только экранирует ту часть поверхности катода, которую сама занимает. [22]
Поскольку вероятность разрыва связей экспоненциально зависит от величины перенапряжений, то очевидно, насколько сильное воздействие на кинетику этого процесса будет оказывать изменение перенапряжений во времени. [23]
Если проводить измерения / при разных значениях Т и т, можно получить серию прямых, по наклонам которых судят об изменении Лэф с изменением перенапряжения. Высокая энергия активации ( свыше 10 ккал / моль) и уменьшение ее с ростом перенапряжения свидетельствует о затруднениях стадии разряда. Низкая энергия активации ( 3 - 5 ккал / моль) и ее постоянство с изменением перенапряжения характерны при затруднениях, связанных с замедленностью диффузии. [24]
Если проводить измерения / при разных значениях Т и т), можно получить серию прямых, по наклонам которых судят об изменении ЛЭф с изменением перенапряжения. Высокая энергия активации ( свыше 10 ккал / моль) и уменьшение ее с ростом перенапряжения свидетельствует о затруднениях стадии разряда. Низкая энергия активации ( 3 - 5 ккал / моль) и ее постоянство с изменением перенапряжения характерны при затруднениях, связанных с замедленностью диффузии. [25]
С другой стороны, i ограничена ROM 0 03 OM-CMZ постольку, поскольку при падении потенциала Де Шом в электролите, которое значительно больше, чем изменение перенапряжения Ат ] - 0 2 в при достижении переходного времени тр, это изменение перенапряжения трудно или совсем невозможно измерить. [26]
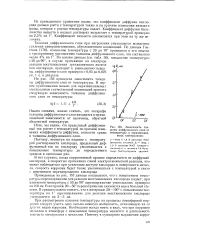 |
Зависимость толщины диффузионного слоя от температуры в неразмешиваемых электролитах. [27] |
В тех случаях, когда коррозионный процесс определяется не диффузией кислорода, а скоростью протекания самой электрохимической реакции, что может наблюдаться при усиленном доступе кислорода к поверхности металла, скорость коррозии будет также увеличиваться с температурой в связи с изменением перенапряжения кислорода. [28]
С другой стороны, i ограничена ROM 0 03 OM-CMZ постольку, поскольку при падении потенциала Де Шом в электролите, которое значительно больше, чем изменение перенапряжения Ат ] - 0 2 в при достижении переходного времени тр, это изменение перенапряжения трудно или совсем невозможно измерить. [29]
Так, например, цементация, подчиняющаяся кинетике типа ( 1), соответствует коррозии двух контактирующих металлов, лимитируемой только электрохимическими факторами. Изменение перенапряжения - коррозионного процесса в зависимости от площадей катода и анода совпадает с изменением компромиссного потенциала в ходе контактного выделения металлов. [30]
Страницы: 1 2 3 4