Изменение - перенапряжение
Cтраница 3
Исследование природы катодной поляризации при осаждении сурьмы в солянокислых растворах [ 50а ] показало, что смещение катодного потенциала IB отрицательную сторону при увеличении концентрации НС1 и в положительную при увеличении содержания сурьмы обусловлено изменением лишь равновесного потенциала. Изменение перенапряжения при увеличении концентрации ионов сурьмы от 0 1 до 0 5 М составляет всего 8 - 10 мв. [31]
Специфические ионные эффекты и, в частности, специфическую адсорбцию катионов следует рассмотреть более подробно. Изменение перенапряжения Дт ] при переходе от чистой соляной кислоты к смеси кислоты с хлоридом щелочного металла возрастает по абсолютной величине в ряду от лития к цезию. [32]
Экспериментальные данные показали, что в области потенциалов, в которой возможна адсорбция поверхностно-активных веществ на поверхности ртути, действительно наблюдается изменение перенапряжения выделения водорода. Сопоставление значений изменения перенапряжения в результате введения добавок с величиной адсорбционного пстенциала ( j) показало, что имеет место полуколичественное совпадение теории с результатами измерений. Это обстоятельство объясняется частичной десорбцией вещества с поверхности электрода при определенных значениях потенциалов. Молекулярные же добавки действуют слабее в результате того, что молекула в этом случае не создает вокруг себя поля, а только экранирует ту часть поверхности катода, которую сама занимает. [33]
 |
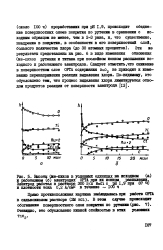
Внутренние напряжения и перенапряжения ряда металлов. [34] |
Отсюда следует, что металлы, осаждающиеся с высоким перенапряжением, должны обладать высокими внутренними напряжениями и наоборот. В ней дано изменение перенапряжения и внутренних напряжений при осаждении ряда металлов из различных солей. [35]
Очень активный гидроксильный радикал быстро реагирует дальше - может быть при содействии поверхностных окислов анода - и, в конце концов, образуется молекулярный кислород. Следовательно, эта часть поляризационной кривой показывает изменение перенапряжения кислорода, предполагая, что в сравниваемых опытах обратимый потенциал, кислорода практически не изменялся. [36]
Кроме того, при продолжительном электролизе часто наблюдали изменения величины Ь, которые были обычно связаны с изменением природы и состояния поверхности. Иногда такие изменения можно непосредственно наблюдать, иногда же изменения перенапряжения имеют своей причиной малые количества примесей в растворе, при продолжительном электролизе дающих на катоде осадок, который у нельзя обнаружить визуально. [37]
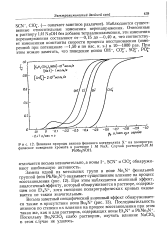 |
Влияние природы аниона фонового электролита Х - на полярографическое поведение хромата в растворе 1 М NaX. Случай раствораО. 01 М. [38] |
Наблюдаются существенные относительные изменения перенапряжения. Отнесенные к раствору IM NaOH без добавок тетраалкиламмония, эти изменения перенапряжения составляют от-0 15 до-0 40 в, что соответствует изменениям константы скорости процесса восстановления ( измеренной при потенциале - 1 50 в по нас. [39]
Учитывая это обстоятельство, необходимо обратиться к другим важным факторам, характеризующим перенапряжение. Такими факторами являются зависимость перенапряжения от природы металла и характер изменения перенапряжения с изменением силы тока. [40]
Здесь отметим лишь, что независимость перенапряжения от концентрации кислоты, наблюдающаяся в действительности лишь для разбавленных растворов кислот в отсутствие индифферентного электролита, была объяснена А. Н. Фрумкиным [2] с помощью представлений о механизме перенапряжения, положенных в основу данной работы. Правильность его убедительно доказывается тем, что оно позволяет полностью объяснить также изменения перенапряжения при введении в раствор нейтральных солей см. статью В. С. Багоцкого п И. Е. Яблоновой в настоящем сборнике, стр. [41]
Эти же результаты представлены на рис. 6 в виде изменения отношения Оже-пкков рутения и титана при послойном ионном распылении исходного и работавшего электродов. Следует отметить что снижение в поверхностном слое ОРТА содержания Ru02 не приводит к изменению перенапряжения реакции выделения хлора. [43]
Согласно этой теории, перенапряжение возникает вследствие накопления атомов водорода на поверхности катода, и изменение перенапряжения при переходе от одного металла к другому приписывается различному каталитическому воздействию этих металлов на скорость соединения атомов водорода в молекулы. Металлы с низким перенапряжением, например платина, палладий, никель и медь, должны быть хорошими катализаторами для реакции 2Н Н2, между тем как металлы с высоким перенапряжением, например свинец, ртуть, олово и кадмий, должны были бы оказаться плохими катализаторами для той же реакции. [44]
 |
Зависимость напряжения на ячейке и его составляющих от температуры при плотности тока, равной 2 кА / м2. [45] |
Страницы: 1 2 3 4