Изменение - положение - равновесие
Cтраница 1
 |
Зависимость набухаемости ( в % солевых форм ионитов от диэлектрической проницаемости ( е растворителей ( вода, метанол, этанол, бутанол, изоамиловый спирт. [1] |
Изменение положения равновесия при переходе от воды к неводным растворителям, особенно в случае мало набухающих форм ионитов, будет определяться не только соотношением зарядов и радиусов обменивающихся ионов и изменением диэлектрической проницаемости, но и степенью отличия состояния ионов в ионите и растворе. [2]
Изменение положения равновесия в результате комплексообразова-ния наблюдается и в случае полиметилбензолов. Например, для три-метилбензолов термодинамическому равновесию в парковой фазе при 100 отвечает, согласно рассчетным данным [25], содержание в смеси 9 % 1 2 3 -, 60 % 1 2 4 - и 31 % 1 3 5-изомеров. Аналогично-пренитол и дурол можно практически полностью превратить в изодурол. [3]
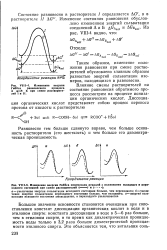
Изменение положений равновесия составных частей молекулы при ее электронном возбуждении характеризуется на графике некоторым смещением потенциальной кривой молекулы относительно кривой нормального состояния и изменением ее формы. [4]
Другой способ изменения положения равновесия состоит в том, что к поверхностным пленкам прилагаются очень высокие давления. [5]
Таким образом, изменение положения равновесия при смене растворителей обусловлено главным образом разностью энергий сольватации изомеров, находящихся в равновесии. [7]
Другой механизм действия поверхностей, приводящий к изменению положения равновесия, состоит в следующем: удаление одного из продуктов реакции в результате избирательной адсорбции может сместить равновесие реакции в сторону образования больших количеств адсорбирующегося компонента. Так, например, при синтезе конденсированного продукта в опытах Уэйстниса и Борсука [ 68а ] ( см. также раздел VI) поверхность, вероятно, действует именно этим путем. [8]
Управление химическим процессом можно осуществлять, применяя различные физические и физико-химические факторы, способные вызвать изменение положения равновесия реакции, ее скорости или направления. [9]
В рассматриваемом случае спирты существуют практически полностью в виде комплексов ( возможно, типа ROA1C12); этим, по-видимому, и объясняется изменение положения равновесия по сравнению с приведенным на рис. 2 - 18, Б, так как образование комплекса по кислороду, а также дополнительная сольватация во много раз увеличивают объем ВОА1Х2 по сравнению с ROH. [10]
Основными недостатками одноплечих весов являются: большие ( по сравнению с равноплечими весами как двухчашечными, так и одночашечными) влияния аэростатистических сил, как за счет невозможности уравновешивать тару материалом одинаковой с ней плотности, так и за счет изменения положения нулевого равновесия; большее влияние температуры на цену деления; повышенный износ призм и подушек; трудность унификации деталей и узлов для обеспечения выпуска различных модификаций весов. [11]
Регулировочными винтами, упирающимися в сходящиеся к лезвию грани призмы, один конец грузо-яриемной призмы незначительно перемещают в горизонтальной плоскости до тех пор, пока ее лезвие не будет параллельно лезвию опорной призмы. Этот момент юстировщик отмечает по прекращению изменений положения равновесия коромысла пр. Операции установки оптической шкалы в двух-призменных и равноплечих весах ( рис. 105) в принципе ничем не отличаются. На рис. 105, а показана шкала двухпризменных ве - - сов, имеющая 100 отсчет-ных делений. [12]
Реакция в паровой фазе также может быть выражена схемой ( 30) [13]; для 327 С имеем К 3 6 и тогда получаем для атмосферного давления Чот - 26 5 ккал / молъ. Здесь величина qoin резко изменяется в результате изменений положения равновесия и соответствующих концентраций. [13]
По смыслу этот параметр аналогичен коэффициенту Бренстеда для переноса протона. Изменение потенциала соответствует изменению равновесия между окисленной и восстановленной формами вещества, подобно тому как изменение рК соответствует изменению положения протолити-ческого равновесия. Величина а показывает, в какой мере потенциал влияет на скорость прямой реакции, и легко определяется из наклона поля-рограмм. [14]
Свободная энергия растянутой формы может быть больше, чем свободная энергия спирально изогнутой формы, поэтому, если оставить материал в растянутом состоянии, молекулы вещества будут стремиться самопроизвольно вернуться к изогнутой форме. В процессе сокращения молекул затраченная на растяжение энергия возвращается не полностью. Этот случай является не чем иным, как химической реакцией с изменением положений равновесия, обусловленным действием приложенного извне напряжения. [15]
Страницы: 1 2