Стремление - атом
Cтраница 2
Оно отражает стремление атомов элементов к образованию электронного октета. Свинец представляет исключение из этого правила; он кристаллизуется в решетке кубической плотной упаковки. [16]
Это объясняется стремлением атомов довести число электронов на внешней оболочке до восьми, что обеспечивает наибольшую ее устойчивость. Внешняя оболочка теряет все электроны ( переход атома в катион) или присоединяет к себе новые электроны ( переход атома в анион), доводя их число до восьми. Так, в кристаллах каменной соли ( NaCI) катион натрия и анион хлора получаются вследствие того, что атом натрия передает свои последний электрон атому хлора, образуя при этом свои восьмиэлектронные внешние оболочки. Заряженные атомы создают ионную решетку кристалла, основанную на силах электростатического взаимодействия. Такая схема связи характерна для большинства солей металлов и их окислов. [17]
Идея о стремлении атомов к образованию общей электронной пары за счет одиночных электронов каждого из двух реагирующих атомов была положена в основу объяснения способа образования ковалентной связи. В соответствии с этим возникло представление о валентности, измеряемой числом одиночных электронов, идущих на образование общих электронных пар. Здесь валентность выражается только числовым значением, без знака. [18]
Под электроотрицательностью понимают стремление атома оттягивать на себя электроны от соседних атомов. Разработаны различные количественные оценки этой величины относительно атома водорода, у которого электроотрицательность принята за ноль. Установлено, что если электроотрицательности элементов, образующих связь, отличаются больше, чем на 1 7, то реализуется ионная связь, а если разница элек-троотрицательностей меньше 1 7 - образуется ковалентпая связь. У галогенов и углерода разница электроотрицателъностей невысока, поэтому между этими атомами образуется полярная ковалентпая связь. [19]
Под электроотрицательностью понимают стремление атома оттягивать на себя электроны от соседних атомов. Разработаны различные количественные оценки этой величины относительно атома водорода, у которого электроотрицательность принята за ноль. Установлено, что если электроотрицательное элементов, образующих связь, отличаются больше, чем на 1 7, то реализуется ионная связь, а если разница злек троотрицательностей меньше 1 7 - образуется ковалентная связь. У галогенов и углерода разница электроотрицательностей невысока, поэтому между этими атомами образуется полярная ковалентная связь. [20]
В этих примерах стремление атома брома занять третичное положение в процессе никакой роли не играет и исключительное влияние следует приписать стремлению углеродных атомов перейти из неустойчивой группировки в другую, более устойчивую, а отсюда следует заключить, что и при бромгидринах с открытыми цепями углеродных атомов изомерный процесс, если не исключительно, то главнейшим образом, обусловливается той же причиной. С другой стороны, так как нестойкость циклических группировок углеродных атомов зависит от имеющихся между последними в большей или меньшей степени натяжений связей, сказывающихся в реакциях присоединения, то следует признать, что и при открытых цепях углеродных атомов, в тех случаях когда в частице имеется третичный радикал, между четвертичным углеродом и примыкающими к нему четырьмя другими углеродами существуют также натяжения связей, которыми не только обусловливается способность такого рода частиц к изомерным превращениям, по в некоторых, пока исключительных случаях, как например при гексафенилэтапе, и к реакциям присоединения. Таким образом, изомерные превращения как циклических соединений, так и соединений с открытыми цепями углеродных атомов объединяются одной общей причиной, и циклические группировки теряют свои специфические свойства. [21]
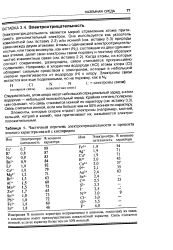 |
Частичный перечень электроотрицательности и процента ионного характера связей с кислородом. [22] |
Электроотрицательность является мерой стремления атома притягивать дополнительный электрон. Она используется как указатель ковалентной ( см. вставку 2.2) или ионной ( см. вставку 3.3) природы связи между двумя атомами. Когда атомы, из которых состоит соединение, разнородны, связи становятся прогрессивно полярными. Например, в хлористом водороде ( HCI) атомы хлора ( CI) обладают сильным сродством к электронам, которые в небольшой степени притягиваются от водорода ( Н) к хлору. [23]
Во всех этих случаях стремление атомов соединиться в молекулы проявляется в распределении или, соответственно, в смещении валентных электронов, так что образуются упорядоченные группы, отвечающие строению благородного газа. Эти группы у водорода состоят из. [24]
Образование ионной связи вызвано стремлением атома к приобретению устойчивой оболочки с полным числом электронов во внешнем слое, как у благородных газов. Например, атом Na ( № 1 1 по системе Менделеева) имеет две заполненные оболочки с числом электронов 2 8 и один электрон на внешнем уровне, который он стремится отдать, а атом С1 имеет 7 электронов на внешней оболочке - ему не хватает одного электрона, чтобы приобрести конфигурацию, как у аргона. [25]
Наличие обменной энергии делает понятным стремление атомов установиться так, чтобы их спины были параллельны или антйпа-раллельны. Очевидно, обменная энергия взаимодействия у ферромагнетиков выходит на первый план и диктует веществу такое расположение спинов, которое приводит к ее минимальному значению. Видимо, у остальных парамагнитных веществ другие слагаемые энергии взаимодействия не дают проявиться обменной энергии. [26]
Наличие обменной энергии делает понятным стремление атомов установиться так, чтобы их спины были параллельны или антипараллельны. Очевидно, обменная энергия взаимодействия у ферромагнетиков выходит на первый план и диктует веществу такое расположение спинов, которое приводит к ее минимальному значению. Видимо, у остальных парамагнитных веществ другие слагаемые энергии взаимодействия не дают проявиться обменной энергии. [27]
В основе теории Косселя лежит стремление атомов отдавать или приобретать при ионизации столько электронов, чтобы образовалась внешняя электронная оболочка, идентичная оболочке атомов соседних благородных газов. Действительно, электронная оболочка последних отличается особенно большой устойчивостью, что видно, например, из их полной химической инертности. [28]
Направленность ковалентной связи является результатом стремления атомов к образованию наиболее прочной связи за счет возможно большей электронной плотности между ядрами. Это достигается при такой пространственной направленности перекрывания электронных облаков, которая совпадает с их собственной. Исключение составляют s - электронные облака, поскольку их сферическая форма делает все направления равноценными. [29]
Более точно можно сказать, что стремление атомов, молекул или ионов найти положение с минимумом энергии обусловливает заселенность грани частицами. Из рис. 6 - 34 очевидно, что число узлов решетки в каждом ряду для различных плоскостей значительно различается. Таким образом, в соответствии со сказанным выше возможность появления и развития грани кристалла в какой-то мере пропорциональна плотности ее сетки и можно предсказать, какие именно грани будут важнейшими в отношении развития и частоты появления в кристалле. [30]
Страницы: 1 2 3 4