Стремление - металл
Cтраница 1
Стремление металлов перейти из металлического в ионное состояние характеризуется величиной уменьшения свободной энергии ( AG) и составляет сущность процессов химической коррозии. [1]
Стремление металлов перейти из металлического в ионное состояние характеризуется величиной уменьшения свободной энергии ( Д ( 7) и составляет сущность процессов химической коррозии. [2]
Стремление металлов перейти из металлического в ионное состояние характеризуется величиной уменьшения свободной энергии ( AG) и составляет сущность процессов химической коррозии. [3]
Стремление металлов переходить из металлического состояния в ионное весьма различно для разных металлов и в общем случае характеризуется величиной уменьшения свободной энергии при протекании соответствующей коррозионной реакции в данных условиях. [4]
Стремление металлов к переходу в ионное состояние зависит как от данного металла, так и от характера коррозионной среды и внешних условий, и может быть охарактеризовано изменением свободной энергии при протекании соответствующей коррозионной реакции в рассматриваемых условиях. [6]
Наряду со стремлением металла отщеплять свои ионы, проявляется стремление раствора осаждать ионы металла на поверхности металла. [7]
Горючесть обусловливается незначительной теплопроводностью порошков, а также стремлением металлов к образованию стабильных окислов. [8]
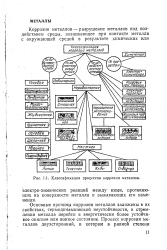 |
Классификация процессов коррозии металлов. [9] |
Основные причины коррозии металлов заложены в их свойствах, термодинамической неустойчивости, в стремлении металла перейти в энергетически более устойчивое окисное или ионное состояние. [10]
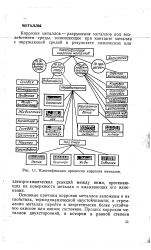 |
Классификация процессов коррозии металлов. [11] |
Основные причины коррозии металлов Заложены в их свойствах, термодинамической неустойчивости, в стремлении металла перейти в энергетически более устойчивое окисное или ионное состояние. [12]
По теории перегруппировки в солях нитрофенолов благодаря положительному щелочному металлу почти полностью восстановлена ациформа, соответственно стремлению металла связаться с отрицательно заряженным местом молекулы. [13]
На аноде же происходит растворение металла с образованием его ионов, следовательно, концентрация ионов металла у анода повышается, стремление металла перейти в раствор уменьшается и электродный потенциал на аноде становится менее элек-роотрицательным. [14]
Для большинства металлов металлич. Стремление металлов переходить из металлич. [15]
Страницы: 1 2 3
