Строение - жидкость
Cтраница 1
Строение жидкостей и тепловое движение в них не поддаются простому описанию. Среднее время t оседлой жизни молекул около временных центров равновесия убывает с ростом температуры. Существует некоторая упорядоченность и в расположении соседних молекул. [1]
Строение жидкостей определяется в основном химическими взаимодействиями между атомами, молекулами или ионами. Нередко существенную роль играет притяжение между ионами или полярными молекулами и окружающей жидкой средой. Химические взаимодействия сопровождаются обобществлением электронов. Они приводят к образованию ассоциатов и комплексов. Химические взаимодействия могут быть сильными, порядка 102 - 103 кДж / моль, и слабыми, порядка 1 - - 10 кДж - моль. [2]
Строение жидкостей и жидких растворов нередко трактуют при помощи понятия ассоциация. Представление об ассоциации но отличается полной определенностью, так как различные авторы нередко вкладывают в термин ассоциация разный смысл. [3]
Строение жидкостей и жидких растворов нередко трактуют при помощи понятия ассоциация. Представление об ассоциации не отличается полной определенностью, так как различные авторы нередко вкладывают в термин ассоциация разный смысл. [4]
Строение жидкости существенно отличается от строения газа, молекулы которого находятся далеко одна от другой и лишь изредка сталкиваются, В жидкости молекулы постоянно находятся в непосредственной близости. Молекулы жидкости расположены как картофелины в мешке. Правда, с одним отличием - молекулы жидкости находятся в состоянии непрерывного хаотического теплового движения. Из-за большой тесноты они не могут передвигаться так свободно, как молекулы газа. Каждая топчется все время почти на одном и том же месте в окружении одних и тех же соседей и только понемногу перемещается по объему, занятому жидкостью. [5]
Строение жидкости существенно отличается от строения газа, молекулы которого находятся далеко одна от другой и лишь изредка сталкиваются. В жидкости молекулы постоянно находятся в непосредственной близости. Молекулы жидкости расположены как картофелины в мешке. Правда, с одним отличием - молекулы жидкости находятся в состоянии непрерывного хаотического теплового движения. Каждая топчется все время почти на одном и том же месте в окружении одних и тех же соседей и только понемногу перемещается по объему, занятому жидкостью. [6]
Строение жидкости существенно отличается от строения газа, молекулы которого находятся далеко одна от другой и лишь изредка сталкиваются. В жидкости молекулы постоянно находятся в непосредственной близости. Молекулы жидкости расположены, как картофелины в мешке. Правда, с одним отличием - молекулы жидкости находятся в состоянии непрерывного хаотического теплового движения. Из-за большой тесноты они не могут передвигаться так свободно, как молекулы газа. Каждая топчется все время почти на одном и том же месте в окружении одних и тех же соседей и только понемногу перемещается по объему, занятому жидкостью. Чем более вязкая жидкость, тем это перемещение медленней, Но даже в такой подвижной жидкости, как вода, молекула сместится на 3 А за то время, которое нужно газовой молекуле для пробега в 700 А. [7]
Такое дырочное строение жидкости справедливо, очевидно, лишь в области не слишком высоких температур и давлений. Вблизи критической температуры средняя плотность жидкости становится настолько малой, что понятие дырок вообще утрачивает свой смысл, подобно тому, как теряется представление о свободном объеме в случае газообразного состояния вещества. В последнем случае дырки сливаются в единое свободное пространство, в которое как бы вкраплены отдельные молекулы. Кроме того, в этом состоянии силы сцепления между частицами становятся столь небольшими, что не могут обеспечить не только правильного, но и вообще сколько-нибудь компактного расположения частиц. [8]
Особенности строения жидкостей определяются факторами ближнего и дальнего порядка. Эффекты дальнего порядка требуют учета коллективного влияния большого числа частиц. Эффекты ближнего порядка, по-видимому, главным образом связаны с парным взаимодействием частиц, образующих жидкость, и их можно изучать с помощью упрощенных моделей, в которых не учитывается окружение каждой такой пары. Для их исследования могут быть с успехом применены квантово-химические методы. [9]
Теория кристаллоподобного строения жидкостей предполагает, что молекулы ( а также атомы или ионы) колеблются около своих положений равновесия. Однако эти положения не фиксированы. Может оказаться, что в результате флуктуации вблизи какой-либо молекулы образуется свободное место ( вакансия), куда эта молекула перескакивает. В результате возникает новое положение равновесия, около которого колеблется молекула. Поскольку вязкость жидкостей гораздо меньше вязкости твердых тел, а скорость диффузии и миграции ионов в жидкости гораздо больше, чем в твердом теле, то частота этих перескоков должна быть относительно большой. [10]
О строении жидкостей известно немного. Подвижность жидкости свидетельствует о том, что ее молекулы могут свободно перемещаться, причем длина среднего свободного пробега молекул очень мала. Из свойства сохранять определенный объем следует сделать вывод, что между молекулами жидкости действуют уравновешивающиеся силы взаимного притяжения и отталкивания. Исследования показывают, что размещение молекул в жидкости не хаотично, а отдаленно напоминает расположение молекул в кристаллической решетке, только оно гораздо менее правильное и с довольно большими пространствами, не заполненными молекулами. [11]
Указанная картина строения жидкости хорошо согласуется с опытными данными по сжимаемости жидкостей: при малых давлениях жидкости в 10 - 15 раз более сжимаемы, чем твердые тела. Это объясняется более рыхлой ( пористой) структурой жидкостей. При больших внешних давлениях порядка тысяч атмосфер сжимаемость жидкостей близка к сжимаемости твердых тел. Для таких состояний дырочная теория строения жидкостей неприменима. Не применима она также к жидкостям, находящимся при высоких температурах, близких к критической. При этих температурах жидкость настолько разрыхлена, что по своей структуре и свойствам близка к газу, для которого понятие дырок не имеет смысла. [12]
Для объяснения строения жидкостей часто используются кривые радиального распределения электронной плотности, получаемые методом рент-геноструктурного анализа. [13]
Ячеечная модель строения жидкостей предполагает, что каждая молекула временно удерживается в равновесном положении потенциальным полем окружающих молекул. При одной и той же температуре все молекулы имеют одинаковую кинетическую энергию - поэтому более тяжелые молекулы обладают большим ко -, личеством движения. [14]
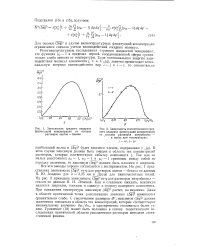 |
Зависимость среднего квадрата.| Зависимость статистического среднего квадрата флюктуации концентрации от остава растворов нитробензол - н. октан при температурах. [15] |
Страницы: 1 2 3 4