Строение - фенол
Cтраница 1
Строение фенолов обусловливает их функциональность, которая определяется числом атомов водорода, способных взаимодействовать с альдегидом. Реакционноспособными являются атомы водорода, находящиеся в орто - и пара-положениях к гидроксильной группе. [1]
Строение фенола определяет его свойства. [2]
Более подробно влияние строения фенолов на коэфиционт распределения было изучено для бутилацетата. [3]
Инфракрасные спектры позволили подметить такие тонкости строения фенолов, которые не доступны наблюдению иными способами. [4]
В первую очередь было изучено влияние строения фенолов на их реакционную способность, причем в фенолах варьировалось число нитрогрупп и их положение в кольце. Концентрации фенолов составляли 0 1 - 0 2 моль / л и при исследовании температурной зависимости констант k для каждого фенола сохранялись постоянными. В табл. 42, приведены значения предэкспоненциальных множителей ku и энергий активации е, рассчитанных по методу наименьших квадратов, для всех исследованных фенолов: В качестве растворителя в этих случаях использовался бензол, а для незамещенного фенола - толуол. [5]
Течение реакций конденсации в значительной степени зависит от строения фенолов ( наиболее энергично реагируют с формальдегидом фенолы, у которых орто - и пара-положения не заблокированы заместителями), а также от соотношения компонентов. [6]
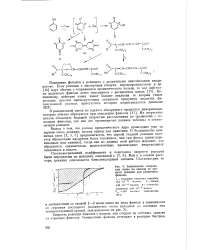 |
Зависимость содержания озона на выходе от времени реакции для различных фенолов. [7] |
Скорость реакции фенолов с езоном, как следует из таблицы, зависит от строения фенолов. [8]
Скорость реакции с роданом еще в большей мере, чем реакция с галоидами, зависит от строения фенолов. Достаточно быстро реагируют фенолы, у которых свободно пара-положение по отношению к гидроксильной группе. Крезол, 2 4-ксиленол реагируют весьма медленно и не мешают определению перечисленных выше фе - нолов. Сам фенол и гваякол занимают промежуточное положение. [9]
Эти реакции, подобно взаимодействию фенола с озоном, протекают с отрывом водорода от оксигруппы фенола и естественно предполагать, что влияние строения фенолов на их реакционную способность во всех случаях будет описываться сходными закономерностями. Значения констант скоростей реакции фенола с 02, а, а - дифенилпикрилгидразилом, пероксирадикалами и озо - - ном приведены в табл. 7.3 ( графы 3, 4, 5 и 6 соответственно), из которой следует, что они довольно хорошо согласуются друг е другом. Поскольку энергии активации всех реакций малы и близки друг к другу ( Ядфпг 5; ERo - 3 - - 4; Ео ж 3 0 ккал / молъ), указанный ряд мало зависит от температуры. [10]
При действии хлорида железа ( III) на одноатомные и многоатомные фенолы в водном нейтральном или слабокислом растворах возникают характерные окраски, не находящиеся, однако, в определенной зависимости от строения фенолов. [11]
При действии хлорида железа ( III) на одноатомные и многоатомные фенолы в водном нейтральном или слабокислом растворах возникают характерные окраски, не находящиеся, однако, в определенной зависимости от строения фенолов. [12]
 |
Величины hRf некоторых фенолов в двух растворителях. [13] |
Хроматографическое поведение многочисленных фенолов, фенолкарбо-новых кислот, фенолальдегидов, диметилфенолов и двухъядерных фенолов исследовано Пастуской и Петровичем на слоях силикагеля Г, приготовленных вручную ( толщина около 0 5 мм), и результаты этих работ были изложены в обзоре, в котором особое внимание уделено зависимости величины Rf от строения фенола ( ср. Для фенолов и фенолкарбо-новых кислот использовали растворители, указанные в табл. 61; в этой таблице приведены величины hRf некоторых фармацевтически особенно интересных веществ этого класса соединений. [14]
Впервые изучены продукты, кинетические закономерности реакций окисления спиртов и фенолов диоксидом хлора в органических растворителях. Впервые установлено влияние растворителя и строения фенолов на кинетику реакции окисления. [15]
Страницы: 1 2