Электронное строение - молекула
Cтраница 1
Электронное строение молекул в ряде случаев не удается удовлетворительно передать с помощью обычных классических структурных формул. Например, классические формулы молекулы H-F или Na-Cl явно недостаточны для понимания свойств этих соединений. Чтобы скомпенсировать этот недостаток графических формул, их разными способами модифицируют. [1]
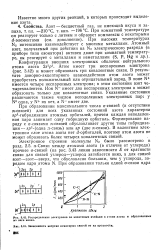 |
Распределение электронов по квантовым ячейкам в атоме азота И образованных из него ионах. [2] |
Электронное строение молекулы N2 было рассмотрено в разд. [3]
 |
Распределение электронов по орбиталям в атоме азота и образованных из него ионах. [4] |
Электронное строение молекулы N2 рассмотрено в разд. [5]
Электронное строение молекулы N0 рассмотрено в разд. [6]
 |
Распределение электронов по орбиталям в атоме азота и образованных из него ионах. [7] |
Электронное строение молекулы N2 рассмотрено в разд. [8]
Электронное строение молекулы СО рассмотрено на стр. [9]
Электронное строение молекулы СО рассмотрено на стр. [10]
Электронное строение молекулы NO было рассмотрено ранее ( см. разд. [11]
Электронное строение молекулы водорода рассмотрено в разд. В лаборатории водород легко получить реакцией между кислотой, например серной H2S04, и металлом, например цинком. [12]
Электронное строение молекулы СО рассмотрено на стр. [13]
Электронное строение молекулы СО рассмотрено в разд. В молекуле образуется тройная связь высокой прочности. [14]
Электронное строение молекулы NO рассмотрено в разд. [15]
Страницы: 1 2 3 4