Геометрическое строение - молекула
Cтраница 2
В методе ВС для предсказания геометрического строения молекул типа AB / t, где п 1, и значений валентных углов применяют предложенную Полингом идею гибридизации АО. [16]
Другой характеристикой химической связи, отражающей геометрическое строение молекулы, является валентный угол. Валентный угол - это угол, образованный линиями, соединяющими центры атомов в направлении действия между ними химической связи. [17]
С помощью электронографии удается непосредственно определить геометрическое строение молекулы, положение отдельных атомов, междуатомные расстояния. При электронографическом анализе некоторых смазок на металлических поверхностях было установлено определенное соответствие между строением слоя смазки и смазывающим действием. [18]
Другой характеристикой химической связи, отражающей геометрическое строение молекулы, является валентный угол. Валентный угол - это угол, образованный линиями, соединяющими центры атомов в направлении действия между ними химической связи. [19]
В книге рассматриваются основы методов опреде ления геометрического строения молекул и кристаллов. Особое внимание в книге уделено проблеме надежности и методам уточнения результатов. [20]
 |
Схематическая связь определяемых в газовой электронографии к. [21] |
Газовая электронография в основном применяется для определения геометрического строения молекул. Для двухатомных и относительно простых многоатомных молекул ( имеются в виду молекулы с высокой симметрией и небольшим числом параметров) может быть достигнута высокая точность-определения - до 10 - 4 нм. В случае сложных молекул различные параметры в принципе определяются с неодинаковой точностью. Поэтому при исследовании ряда молекул некоторые параметры найдены с очень высокой точностью, например г ( С - Н), г ( С-С) и Z. [22]
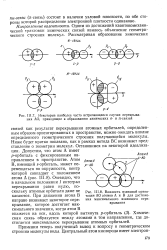
Применим теперь полученный вывод к вопросу о геометрическом строении молекулы воды. [24]
 |
Валентные углы в некоторых молекулах. [25] |
Важно подчеркнуть, что выводы теории ОЭПВО о геометрическом строении молекул легко экстраполируются на более сложные молекулы и ионы, чем рассмотренные в табл. 10.3 - 10.5. В каждом случае необходимо выделить фрагмент, содержащий центральный атом, координирующий около себя другие атомы или их группировки, и установить число и тип окружающих данный атом электронных пар. Каждый атом фосфора в ней имеет три соседа и, кроме того, сохраняет одну неподеленную электронную пару. [26]
Классификация структурных фрагментов обычно проводится па основе анализа данных по геометрическому строению молекул некоторого ряда и представлений о характере взаимодействия отдельных структурных групп в молекуле друг с другом либо на основе анализа изменений термодинамических функций при реакциях между молекулами ряда, в частности при реакциях диспро-порционирования. В большинстве опубликованных работ используется одно из трех нижеперечисленных направлений: 1) классификация по типам атомов; 2) классификация по типам связей групп атомов: 3) классификация но различным попарным взаимодействиям атомов и связей. Каждая конкретная схема содержит определенные предположения относительно выбора фрагментов и классификации взаимодействий. [27]
Электронография как экспериментальный метод органической химии применяется главным образом для определения геометрического строения молекул. [28]
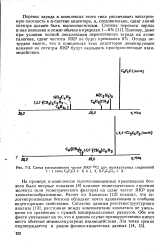 |
Схема расположения частот ЯКР 35С1 для молекулярных соединений 1. 1 типа C6F5C1 X и 1, 3, 5 - Р3С6С13 X. [29] |
На примере я-комплексов галогензамещенных производных бензола было впервые показано [4] влияние геометрического строения молекул ( или геометрического фактора) на сдвиг частот ЯКР при комплексообразовании. Расчет по Хюккелю [12] показал, что га-логенпроизводные бензола обладают почти одинаковыми и слабыми акцепторными свойствами. Согласно данным рентгеноструктурного анализа [13], расстояние между компонентами комплекса не уменьшено по сравнению с суммой вандерваальсовых радиусов. Оба эти факта указывают на то, что в данном случае преимущественно имеют место обычные межмолекулярные взаимодействия. [30]
Страницы: 1 2 3 4