Влияние - изотопное замещение
Cтраница 2
В данном разделе мы подробно рассмотрим одно из таких электронных свойств, а именно дипольный момент. В дальнейшем можно будет обобщить влияние изотопного замещения и на другие свойства, для которых аналогичное рассмотрение было бы значительно более трудоемким. [16]
В формулы типа ( 135) входят только колебательные частоты, которые удается определить спектроскопически, если частицы не слишком сложные. Зная эти частоты, можно предсказать влияние изотопного замещения на простые равновесия, что было с успехом сделано для некоторых реакций в газовой фазе. [17]
Доказательство существования промежуточного о-комплекса основано на результатах нескольких направлений исследования. Первый очень информативный подход состоит в измерении влияния изотопного замещения на скорость реакции. Если протон уходит с места замещения синхронно с введением электрофила, то в реакциях, в которых, злектро-фильная атака кольца определяет скорость реакции, должен Наблюдаться первичный изотопный эффект. Этою не наблюдается в реакции нитрования и некоторых других реакциях электрофильного замещения в ароматическом ряду. Отсутствие изотопного эффекта подтверждает тот факт, что протон уходит на быстрой стадии, следующей за стадией, определяющей скорость реакции, и тем самым свидетельствует о наличии интермедиата. Отсутствие первичного изотопного эффекта не является, однако, всеобщим правилом. Существование этих изотопных эффектов свидетельствует в пользу механизма с образованием а-ком-плекса со стадией отрыва протона ( ароматизации), определяющей скорость реакции. Многие из наблюдавшихся умеренных кинетических изотопных эффектов ( кн / кв от 1 2 до 2 0) были интерпретированы с точки зрения сравнимых скоростей образования и разрушения сг-комплекса. [18]
Рассмотренные соображения, справедливые для гомогенных реакций, остаются в силе и для большинства гетерогенных реакций на каталитических поверхностях: при адсорбции энергетические уровни понижаются, но большей частью соотношения между ними качественно остаются теми же. В действительности, как в гомогенных, так и в гетерогенных реакциях влияние изотопного замещения на скорость осложняется рядом дополнительных факторов, которые здесь не рассматривались и в общем виде не поддаются учету. [19]
Изолированное наблюдение различия скорости ферментативно катализируемой реакции в воде и в окиси дейтерия не дает ничего существенного для понимания механизма реакции. Элементарные требования, необходимые для интерпретации изотопных эффектов в ферментативных реакциях, заключаются в следующем: 1) необходимо разделение влияний изотопного замещения на максимальную скорость и на - йГщ с дальнейшим разделением влияний на элементарные константы скоростей и равновесий реакции; 2) необходимо разграничение изотопных эффектов для водородных атомов, необменивающихся и быстро обменивающихся с растворителем; 3) для экспериментов, проводимых в растворах окиси дейтерия, необходимо определение влияния этого растворителя на зависимость максимальной скорости и константы Михаэлиса от кислотности. Изотопные эффекты в реакциях переноса необменивающихся атомов водорода, которые обычно связаны с углеродом, интерпретировать относительно легко, поскольку их можно изучать в растворителе постоянного состава, в то время как протоны, связанные с кислородом, азотом или серой, всегда обмениваются с растворителем с диффузионно контролируемой скоростью, которая много выше, чем у изучаемой реакции; дейтериевый изотопный эффект в таких реакциях необходимо изучать при использовании окиси дейтерия в качестве растворителя, что влечет за собой определенные трудности в интерпретации результатов, связанных с влиянием растворителя. [20]
В данной работе изучено влияние замещения водорода, образующего водородную связь, дейтерием на давление пара и энтальпию парообразования, вязкость, растворимость и энтальпию растворения, осмотические коэффициенты, мольный объем, сжимаемость, критическую температуру и поляризуемость молекул ряда одноатомных спиртов, этиленгликоля, глицерина, некоторых гидроперекисей и карбоновых кислот. Кроме того, исследованы и сопоставлены изотопные эффекты в свойствах, вызываемые замещением водорода дейтерием в амино-группе анилина, в его ароматическом кольце, а также во всей молекуле. Для сравнения изучено влияние изотопного замещения на свойства ряда неассоциированных веществ. [21]
Данная статья построена скорее по логическому принципу, нежели по хронологическому. Порядок изложения характерен для классической физической органической химии. Вначале будет рассмотрено влияние изотопного замещения на электронные свойства молекул, тесно связанные с их химической реакционной способностью. Далее будет разобрано, каким образом вторичные изотопные эффекты укладываются в общую теорию изотопных эффектов, а также в какой степени выводы формальной теории согласуются с интуитивными положениями ученого-специалиста в области физической органической химии. Только после этого в порядке возрастания сложности материала будут эмпирически рассмотрены экспериментальные данные, причем каждая серия экспериментальных данных будет по мере возможности связываться с теорией. [22]
При средних или повышенных температурах ( для многоатомных жидкостей) уменьшение энергии межмолекулярных колебаний в результате замещения легкого изотопа тяжелым вызывает увеличение энергии разрыва межмолекулярных связей, а уменьшение энергии ван-дер-ваалъсо-вого взаимодействия при таком замещении вызывает уменьшение энергии разрыва межмолекулярных связей. Выше показано, что разность энергии колебаний изотопных молекул сравнительно быстро уменьшается с ростом температуры и молекулярного веса. Поэтому в области стандартной термодинамической температуры влияние изотопного замещения на энергию разрыва межмолекулярных связей неассоциированных жидкостей обычно определяется различием энергии ван-дер-ваальсового взаимодействия изотопных молекул. Это подтверждается тем, что разности теплот парообразования некоторых дейтеропроизводных углеводородов и их соответствующих обычных аналогов, рассчитанные по экспериментальным данным о температурной зависимости давления пара, близки к разностям ван-дер-ваальсовой энергии для тех же соединений, рассчитанным как описано выше. [23]
Статья Уилсона и Ханта [28], посвященная пересмотру отнесения спектра SO2F2, знакомит с некоторыми трудностями, возникающими при отнесении. Часто определенное отнесение полос представляется самосогласованным, но оно не всегда однозначно. Дополнительным подтверждением отнесения могут служить исследования влияния изотопного замещения на положение спектральных линий. [24]
По мнению Эйринга [55], теория переходного состояния в своем современном виде не может ( и никогда не была предназначена) уверенно оперировать с теми величинами различий в скоростях реакций, с которыми сталкиваешься при изучении вторичных изотопных эффектов. Тем не менее, если возникает необходимость теоретического рассмотрения подобных эффектов, следует все же воспользоваться теорией кинетических изотопных эффектов, которой, по существу, ограничиваются все наши возможности в настоящее время. К счастью, как указывают Бигеляйзен и Вольфсберг [ 48а ], влияние изотопного замещения на различные количественные характеристики молекул может быть часто предсказано с большей достоверностью, чем сами характеристики. [25]
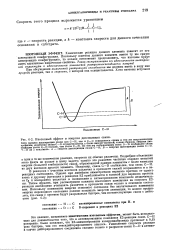 |
Изотопный эффект и энергия диссоциации связи. [26] |
Подробное объяснение этого факта не входит в нашу задачу; однако это различие частично обязано меньшей энергии ( большей стабильности) связи, образованной данным элементом с более тяжелым из двух изотопов другого элемента. В реакциях с участием изотопов различия в прочности связей сохраняются и в переходных состояниях. Однако при линейном симметричном переносе протона от одного атома к другому ( ситуация в реакциях Е2 приближается к таковой для переноса протона от С0 к основанию) различия в связывании в активированном комплексе незначительны. Таким образом, при рассмотрении влияния изотопного замещения на скорость Е2 - реакции необходимо учитывать различия в прочности связи только в основном состоянии. [27]
Большие изотопные эффекты водорода были обнаружены экспериментально вскоре после того, как в 1932 г. был открыт дейтерий. В настоящее время в этой области имеется множество работ, включая исследования с тритием. Значительная часть их посвящена кинетике реакций, сопровождаемых переносом протона. Однако получена большая информация и о влиянии изотопного замещения на термодинамику кислотно-основного взаимодействия. В недавнем [1] обзоре подсчитано, что по изотопным эффектам теперь каждый год публикуется около 300 статей, в основном относящихся исследованию изотопного замещения водорода. Настоящая глава посвящена рассмотрению влияния изотопного замещения на константы кислотно-основного равновесия. Кинетические изотопные эффекты в реакциях переноса протона составляют содержание гл. [28]
Чарльз Фридель и Джеймс Мэзон Крафтс начали свои: классические опыты по замещению атомов водорода, связанных с бензольным кольцом, другими реагентами, которые мы теперь называем электро-филышми. Основная заслуга в раскрытии секретов этих реакций принадлежит Ларсу Меландеру с его изящными экспериментами по изучению влияния изотопного замещения на скорость замещения в ароматическом ряду. [29]
Полоса, которая не сдвигается ( по шкале волновых чисел) при изотопном замещении какого-либо атома, должна принадлежать частице, не содержащей этого атома. Область применения данного правила определяется тем, что в многоатомных молекулах некоторые частоты колебаний при изменении массы одного атома сдвигаются очень мало. Поэтому этот метод наиболее применим для небольших частиц, изотопное замещение в которых значительно изменяет все частоты. Небольшая ширина полос матрично-изолированных молекул делает возможным измерение изотопного сдвига порядка 1 см 1 или даже менее / Таким образом, у небольших молекул можно экспериментально обнаружить влияние изотопного замещения на все полосы, причем величина изотопного сдвига различных полос показывает, какие атомы участвуют в каждом колебании. [30]
Страницы: 1 2 3