Влияние - материал - электрод
Cтраница 4
В качестве материала электродов употреблялась обычно платина и иногда золото, за исключением приводимых ниже специальных опытов по выяснению влияния материала электрода на характер осаждения, где применялись также другие металлы. Электролиз производился обычно в стеклянном сосуде, дно которого было сделано из платиновой фольги и служило электродом. [46]
Природа электрода, так же как и степень развития его поверхности, играет важную роль в кинетике процессов электрохимического восстановления и окисления; особенно отчетливо это проявляется в случае сложных окислительно-восстановительных реакций. Например, при восстановлении азотной кислоты на губчатой меди получается почти исключительно аммиак, а на амальгамированном свинце - преимущественно гидроксиламин. Другим примером влияния материала электрода на процесс электровосстановления может служить реакция восстановления ацетона. [47]
Плюкер [542] установил, что спектр разряда газа, помещенного в герметически закрытую трубку, является характеристическим. Вил-лиген [543] исследовал влияние материала электрода на спектры газов, изучил действие солей металлов, испаряющихся на электродах, а также влияние межэлектродных расстояний. Бунзен [547] начали публиковать первые результаты опытов с первым спектроскопом, положившие начало новой области аналитической химии. [48]
Количество энергии, излучаемое дугой, в сильной степени зависит от материала электродов. Влияние материала электродов на интенсивность излучения может быть объяснено наличием в дуге паров материала электродов, которые дают различные спектры излучения. Следует отметить, что влияние материала электродов на мощность излучения наблюдается при относительно коротких дугах, в которых пары материала электродов распространяются по всему объему ствола дуги. [49]
При таких условиях температура катода может достигать 2000 - 2200 С. На рис. 3.32 приведены зависимости температуры стенок полости и образца от величины разрядного тока. Из рис. 3.33 видно влияние материала электрода и рабочего газа на мощность разряда в полом катоде. Предельная мощность и температура соответствуют максимальному значению напряжения на катодной трубке. [51]
Согласно этой теории наиболее медленной является стадия мо-лизации ( рекомбинации) адсорбированного водорода, поэтому в процессе электролиза концентрация атомного водорода на поверхности увеличивается по сравнению с равновесной, что и приводит к сдвигу потенциала электрода в отрицательную сторону. В дальнейшем эта теория была развита Н. И. Кобозевым, который связал замедление молизации водорода с энергией адсорбции водорода металлом. В рекомбинационной теории впервые было объяснено влияние материала электрода на величину перенапряжения водорода. [52]
Если предположить, что изменение перенапряжения водорода при переходе от Pt к Hg целиком обусловлено изменением энергии адсорбции атомарного водорода, то получается Eng - u 27 ккал / моль. Таким образом, экспериментальные данные подтверждают основные положения теории замедленного разряда о влиянии материала электрода на скорость электрохимической реакции. [53]
 |
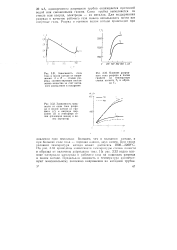
Зависимость элек. [54] |
С увеличением поверхности электродов прочность увеличивается. Прочность жидких диэлектриков увеличивается, если электроды взять из более теплопроводного материала. Влияние материала электродов уменьшается с увеличением чистоты жидкого диэлектрика. [55]
Природа электрода, так же как и степень развития его поверхности, играет важную роль в кинетике процессов электрохимического восстановления и окисления; особенно отчетливо это проявляется в случае сложных окислительно-восстановительных реакций. Найдено, например, что при восстановлении азотной кислоты на губчатой меди получается почти исключительно аммиак, а на амальгамированном свинце - преимущественно гидроксиламин. При плотности тока, равной 0 24 а / см2, на медном катоде 98 5 % тока расходуется на образование аммиака и только 1 5 % - на образование гидроксиламина. Другим примером влияния материала электрода на процесс электровосстановления может служить реакция восстановления ацетона. [56]
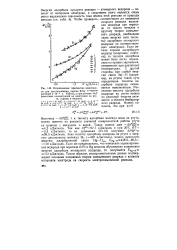 |
Исправленные тафелевские зависимости для восстановления аниона ВгОГ в В ДНОМ растворе 2 - 10 - 4 н. NaBrO4 в присутствии NaF различных концентраций на электродах из ртути, сурьмы и висмута. [57] |
Такая оценка дает - АЯ о 4 2 кДж / моль. Так как Л 0Сб) 97 7 кДж / моль и при 20 С ЯГ 2 4 кДж / моль, то из уравнения (53.13) получаем АЯЦДС 99 5 кДж / моль. Если же предположить, что изменение перенапряжения водорода при переходе от Pt к Hg целиком обусловлено изменением энергии адсорбции атомарного водорода, то получается Еце - н & ж ИЗ кДж / моль. Таким образом, экспериментальные данные подтверждают основные положения теории замедленного разряда о влиянии материала электрода на скорость электрохимической реакции. [58]
Страницы: 1 2 3 4