Влияние - неэлектролит
Cтраница 1
Влияние неэлектролитов на гидродинамическую подвижность ионов при переносе электричества в ряде отношений аналогично влиянию на диффузию ( разд. [1]
Влияние неэлектролита на коэффициент активности соли обычно исследуется при сравнительно высокой концентрации соли, так что имеет место и взаимодействие между ионами самой соли. Этот вк лад в у следует учитывать особо. [2]
Влияние неэлектролитов на проводимость водных растворов электролитов рассмотрено в ряде исследований. В качестве неэлектролитов использовали органические вещества ( например, сахара), а также растворимые в воде или смешивающиеся с ней органические жидкости. [3]
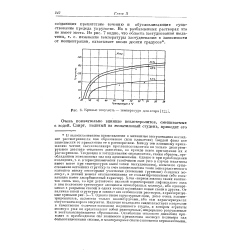 |
Кривые текучесть - температура для arapa [ 122J. [4] |
Очень показательно влияние неэлектролитов, смешиваемых с водой. [5]
В отношении влияния неэлектролитов на водные растворы электролитов наблюдается значительное различие между электролитами, ионы которых мигрируют чисто гидродинамически, и электролитами, ионы которых переносят электричество и по прототропному механизму. В растворах первых электролитов основной механизм миграции не изменяется под влиянием неэлектролитов; изменяются лишь условия переноса электричества. В растворах ионов с прототропной проводимостью присутствие неэлектролита, особенно в большой концентрации, существенно изменяет механизм переноса электричества. Гидродинамическая миграция может подавить гарототропный механизм проводимости, а природа последнего при повышении концентрации неэлектролита в растворе может измениться, если обмен протонов между молекулами неэлектролита будет преобладать над обменом протонов между молекулами воды. Однако влияние неэлектролитов на про-тотропную проводимость трудно отделить от их влияния на гидродинамическую миграцию отчасти потому, что участвующие в прототропной проводимости ионы оксония мигрируют, также по гидродинамическому механизму, и отчасти потому, что другие ионы электролита переносят электричество также в результате гидродинамической миграции. [6]
Также изменяется под влиянием неэлектролитов проводимость растворов крупных ионов. [7]
Высокая чувствительность лиофобных золей к действию электролитов при практически полном отсутствии влияния неэлектролитов привела Гарди к выводу, что устойчивость таких систем обусловлена зарядом частиц и коагуляция наступает в изоэлектри-ческой точке. Оказалось, однако, что в момент коагуляции заряд частиц не равен нулю. Было показано [18- 24], что между влиянием электролитов на - потенциал, с одной стороны, и их коагулирующим действием на коллоидные растворы, с другой, имеется параллелизм. Повис [25] ввел понятие о критическом потенциале, имеющем во всех случаях некоторое постоянное значение, ниже которого наступает быстрая коагуляция. [8]
Тем не менее разни-да между значениями проводимости электролитов, проводящих по механизму гидродинамической миграции и по прото-тропному механизму, и электролитов, проводящих лишь по механизму гидродинамической миграции, дает достаточно надежную информацию об изменениях в прототропном механизме проводимости при добавлении в раствор неэлектролитов, тем более что влияние неэлектролитов на проводимость растворов, проводящих по тому или другому механизму, сильно различается. [9]
В отношении влияния неэлектролитов на водные растворы электролитов наблюдается значительное различие между электролитами, ионы которых мигрируют чисто гидродинамически, и электролитами, ионы которых переносят электричество и по прототропному механизму. В растворах первых электролитов основной механизм миграции не изменяется под влиянием неэлектролитов; изменяются лишь условия переноса электричества. В растворах ионов с прототропной проводимостью присутствие неэлектролита, особенно в большой концентрации, существенно изменяет механизм переноса электричества. Гидродинамическая миграция может подавить гарототропный механизм проводимости, а природа последнего при повышении концентрации неэлектролита в растворе может измениться, если обмен протонов между молекулами неэлектролита будет преобладать над обменом протонов между молекулами воды. Однако влияние неэлектролитов на про-тотропную проводимость трудно отделить от их влияния на гидродинамическую миграцию отчасти потому, что участвующие в прототропной проводимости ионы оксония мигрируют, также по гидродинамическому механизму, и отчасти потому, что другие ионы электролита переносят электричество также в результате гидродинамической миграции. [10]
Эти же представления оказываются весьма полезными и при рассмотрении вопроса о влиянии неэлектролитов на структуру воды. [11]
 |
Результаты определения характеристик гидролиза электролита в водно-органических растворах при 25 С. [12] |
Рассчитывают степень и константу гидролиза, а также AGj гидролиза. Строят график зависимости изменения степени гидролиза от объемной концентрации органического компонента. Делают вывод о влиянии неэлектролита на процесс гидролиза. [13]
 |
Результаты определения характеристик гидролиза электролита в водно-органических растворах при 25 С. [14] |
Рассчитывают степень и константу гидролиза, а также ДСт гидролиза. Строят график зависимости изменения степени гидролиза от объемной концентрации органического компонента. Делают вывод о влиянии неэлектролита на процесс гидролиза. [15]
Страницы: 1 2