Изменение - величина - потенциал
Cтраница 2
Наблюдения за электролизерами, вырабатывающими кислород, загрязненный водородом, показали, что процессы, приводящие к этому, сопровождаются изменением величины потенциала диаф-рагменной рамы ячейки по отношению к потенциалам анода и катода. В нормально работающей ячейке значение потенциала рамы обычно находится примерно посередине между потенциалами анода и катода данной ячейки. [16]
Уменьшение концентрации электролита в растворе должно вести ft изменению соотношения между поверхностной и объемной проводимостью раствора в капилляре, а следовательно и к изменению величины потенциала протекания. Этот случай рассматривается в работах Рутгерса [28] л его школы. [17]
Если электрод находится в насыщенном растворе своей соли, то потенциал его определяется концентрацией катионов в растворе, но изменение концентрации аниона тоже вызывает изменение величины потенциала. Примером может служить серебряный электрод в насыщенном растворе хлористого серебра. [18]
Вне оболочек поле сетки не проникает. Изменение величины потенциала на сетке приводит лишь к небольшому изменению толщины оболочки. Изменение знака потенциала на сетке приводит к изменению знака зарядов в оболочке. [19]
В соответствии с уравнением Нернста для окислительно - восстановленных систем происходит уменьшение величины потенциала, если окисленная форма образует более устойчивый комплекс, чем восстановленная, и, наоборот, увеличение при образовании более устойчивого комплекса восстановленной формы. Изменение величины потенциала, естественно, позволяет определить концентрацию потенциалопределяющих ионов и тем самым константы образования комплексов. [20]
Потенциал разложения электролита изменяется в зависимости от природы электродов. Изменение величины потенциала разложения в зависимости от материала электрода, является результатом различной величины - веляризации. [21]
Растворы, приготовляемые на дистиллированной воде, подвергали магнитной обработке. В опытах исследованы изменение величины потенциала Стали 20 во времени и зависимость скорости реакций, протекающих на электродах ( из Стали 20), от этого потенциала. [22]
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих лолуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [23]
 |
Ряд напряжений металлов. [24] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а эл ек-тродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция закан-чива. [25]
 |
Ряд напряжений металлов. [26] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [27]
 |
Ряд напряжений металлов. [28] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция закан чивается - наступает состояние химического равновесия. [29]
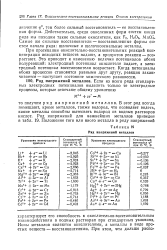 |
Ряд напряжений металлов. [30] |
Страницы: 1 2 3