Изменение - величина - потенциал
Cтраница 3
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [31]
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [32]
 |
Ряд напряжений металлов. [33] |
При протекании окислительно-восстановительных реакций ко иентрацпп исходных веществ падают, а продуктов реакции - во растают. Это приводит к изменению величин потенциалов обе. Когда потенциал обоих процессов становятся равными друг другу, реакция зака. ЧИРлетен - наступает состояние химического равновесия. [34]
 |
Ряд напряжений металлов. [35] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакцида - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [36]
 |
Ряд напряжений металлов. [37] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - возрастают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается-наступает состояние химического равновесия. [38]
 |
Ряд напряжений металлов. [39] |
При протекании окислительно-восстановительных реакций концентрации исходных веществ падают, а продуктов реакции - воз растают. Это приводит к изменению величин потенциалов обеих полуреакций: электродный потенциал окислителя падает, а электродный потенциал восстановителя возрастает. Когда потенциалы обоих процессов становятся равными друг другу, реакция заканчивается - наступает состояние химического равновесия. [40]
Потенциал осаждения металла из комплекса отличается от потенциала выделения металла из простых солей. Координация аддендов ионами металлов-комплексообразователей приводит к изменению величины потенциала выделения металла. Причем потенциал выделения из однотипных комплексов для разных металлов сдвигается в различной степени в зависимости от прочности образующихся комплексов. Поэтому становится возможным электролитическое разделение этих металлов электролизом растворов их координационных соединений. С другой стороны потенциалы осаждения металлов в результате образования комплексов могут быть сближены. Электролиз растворов таких комплексов приводит к выделению сплавов. Например, в присутствии избытка цианид-иона удается электролитически отделить железо от цинка, тогда как при электролизе циаяидсодер-жащих растворов меди и цинка выделяется латунь. [41]
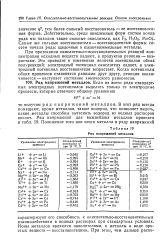
После каждой взятой порции осадителя измеряется разность потенциалов так, как показано выше. По мере титрования при начинающемся увеличении темпа изменения величины потенциалов уменьшают до капель порции вливаемого раствора серебряной соли. Титрование ведут до тех пор, пока изменение потенциала ( отнесенное к единице объема раствора AgNO3) после максимальных значений не станет скова нерезким. Участку, отмеченному максимальным изменением потенциала, отвечает конец титрования брома. Соответствующий объем серебряной соли можно найти или непосредственно по наибольшему значению изменения потенциала, или графически, откладывая на оси абсцисс объем израсходованного раствора серебряной соли ( мл), а по оси ординат - величины компенсирующего напряжения. [42]
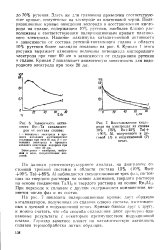
Здесь же для сравнения приведены соответствующие кривые, полученные на электроде из платиновой черни. Поляризационные кривые окисления водорода н восстановления кислорода на сплаве, содержащем 10 % рутения, наиболее близко расположены к соответствующим поляризационным кривым платинового электрода. Кривая / этого рисунка выражает изменение величины потенциала кислородного электрода при токе 60 ма в зависимости от содержания рутения в сплаве. Кривая 2 показывает аналогичную зависимость для водородного электрода при токе 20 ма. [44]
Страницы: 1 2 3