Влияние - неводный растворитель
Cтраница 1
Влияние неводных растворителей сказывается не только в изменении Ддисс. Это обстоятельство значительно расширяет возможность кислотно-основного титрования, так как в неводных растворах можно дифференцированно титровать смеси электролитов, / СДИСс - которых в водном растворе очень близки. [1]
Влияние неводных растворителей сказывается не только в изменении / Сдисс. Это обстоятельство значительно расширяет возможность кислотно-основного титрования, так как в неводных растворах можно дифференцированно титровать смеси электролитов, Кюсс - которых в водном растворе очень близки. [2]
Влияние неводных растворителей, которые часто применяются в органической электрохимии, на величину D и таким образом на диффузионный ток - не однозначно. Обычно применяют смеси растворителей, и в соответствии с отношением компонентов могут быть получены зависимости разного вида при изменении концентрации одного компонента. [3]
Используя влияние неводных растворителей на свойства растворенных электролитов, можно проводить кислотно-основное титрование в неводных средах таких веществ, которые не могут быть оттитрованы в водных растворах. [4]
Рассмотрим влияние неводных растворителей на точность титрования. Точность определения кислот ( или оснований) зависит в первую очередь от их способности к электролитической диссоциации. Сильные кислоты титруются с очень незначительной погрешностью. Выше было показано, что погрешность определения слабых кислот возрастает с уменьшением их констант диссоциации. [5]
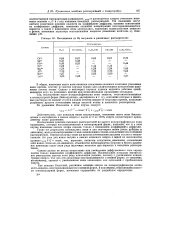 |
Потенциалы ( в В полуволн в различных растворителях. [6] |
Исследования влияния неводных растворителей на высоту полярографических волн папаверина, который восстанавливается в молекулярной форме, показали, что и в этом случае изменение высоты волны связано только с изменением коэффициента диффузии. [7]
Исследование влияния неводных растворителей на высоту волн папаверина, который восстанавливается в молекулярной форме, показали, что и в этом случае изменение высоты волны связано только с изменением коэффициента диффузии. [8]
Исследования влияния неводных растворителей на высоту полярографических волн папаверина, который восстанавливается в молекулярной форме, показали, что и в этом случае изменение высоты волны связано только с изменением коэффициента диффузии. Такие же результаты наблюдались нами и для некоторых ионов ( ионы рубидия и хинолина), мало сольватированных и мало изменяющих степень сольватации под влиянием растворителей. Гентери получил такие же простые соотношения для иона талия в этиленгликоле. Но уже для ионов натрия в смесях этилового спирта с водой не выполняется правило г дИф / т; const, что, вероятно, является следствием изменения сольватации этих ионов. Этим же, по-видимому, объясняется наблюдавшееся Перачио и Мелох различное изменение высот волн ряда щелочных металлов при переходе к неводным растворителям. [9]
Под влиянием неводных растворителей с различной величиной констант автопротолиза сила кислот, оснований и степень диссоциации солей изменяется в неодинаковой степени. Это дифференцирующее действие неводных растворителей используется для титрования смесей, раздельное определение компонентов которых в водной среде невозможно из-за гидролиза продуктов реакций. [10]
Под влиянием неводных растворителей изменяются свойству любых электролитов: кислот, оснований и солей. В зависимости от растворителя одно и то же вещество может быть неэлектролитом, сильным или слабым электролитом, кислотой или основанием или же вовсе не проявлять кислотно-основных свойств. Эта изменчивость свойств веществ под влиянием растворителей может быть с успехом использована для решения ряда аналитических задач: при кислотно-основном титровании, при титровании по методу осаждения, при полярографическом анализе и при других методах анализа. [11]
Под влиянием неводных растворителей изменяются свойства любых электролитов: кислот, оснований и солей. В зависимости от растворителя одно и то же вещество может быть неэлектролитом, сильным или слабым электролитом, кислотой или основанием или же вовсе не проявлять кислотно-основных свойств. Эта изменчивость свойств веществ под влиянием растворителей может быть с успехом использована для решения ряда аналитических задач: при кислотно-основном титровании, при титровании по методу осаждения, при полярографическом анализе и при других методах анализа. [12]
Для объяснения характера влияния неводных растворителей в связи, с составом фона Безуглым было проведено изучение формы электрокапиллярных кривых в зависимости от природы и концентрации отсутствующего электролита, в том числе и от природы аниона. [13]
Для объяснения характера влияния неводных растворителей в связи с составом фона В. Д. Безуглым было произведено изучение формы электрокапиллярных кривых в зависимости от природы и концентрации сопутствующего электролита, в том числе и от природы аниона. [14]
Рассмотренное в предшествующих главах влияние неводных растворителей на кислотно-основные свойства растворенного в них вещества далеко не исчерпывает всего разнообразия эффектов, наблюдаемых в их среде. [15]
Страницы: 1 2 3