Влияние - неводный растворитель
Cтраница 2
Полученные нами данные по влиянию неводных растворителей на вращательную подвижность зонда 5 в эритроцитах в общем аналогичен их влиянию на структуру липосом. [16]
Как уже говорилось выше, влияние неводных растворителей сказывается не только в изменении К, кислот и оснований, но и в изменении соотношения в силе кислот или оснований. Это обстоятельство значительно расширяет возможность кислотно-основного титрования, так как в неводных растворах можно дифференцированно титровать смеси электролитов, К которых в водном растворе очень близки. Возможность раздельного титрования смеси кислот или оснований определяется соотношением / ( HAD, и / КиАп, i или Кв, п / - Кв, т - В среде дифференцирующих растворителей эти соотношения оказываются значительно меньше, чем в водных растворах. [17]
 |
Изменение Др / С кислот в среде различных растворителей. [18] |
Как уже говорилось выше, влияние неводных растворителей сказывается не только в изменении К кислот и оснований, но и в изменении соотношения в силе кислот или оснований. Это обстоятельство значительно расширяет возможность кислотно-основного титрования, так как в неводных растворах можно дифференцированно титровать смеси электролитов, значения К которых в водном растворе очень близки. Возможность раздельного титрования смеси кислот или оснований определяется соотношением / Сндп, п / ДнАп, i или Кв, и / Кв, i - В среде дифференцирующих растворителей эти соотношения оказываются значительно меньше, чем в водных растворах. [19]
Рассмотрены некоторые последние данные по влиянию неводных растворителей на величины предельных диффузионных токов и потенциалов полуволн и на перераспределение электронной плотности молекул восстанавливающихся и образующихся при восстановлении веществ. [20]
Один и тот же электролит под влиянием разнообразных неводных растворителей, характеризующихся различными протолитиче-скими свойствами и разными значениями диэлектрической проницаемости, может быть сильным или слабым электролитом и даже совсем потерять электролитические свойства. Так, а-нафтиламин является слабым основанием ( р / Св 10 01) в водной среде, очень сильным основанием ( р / Гв0 88) в среде безводной муравьиной кислоты ( протогенный растворитель), а в жидком аммиаке и других протофильных растворителях совсем не проявляет основных свойств. [21]
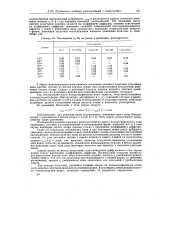 |
Потенциалы ( в В полуволн в различных растворителях. [22] |
ДИф от растворителя следует учитывать изменение величин п, D и с под влиянием неводных растворителей. [23]
В исследованиях последних лет, особенно в работах Н. А. Измайлова, было показано, что под влиянием неводных растворителей изменяются свойства любых электролитов: кислот, оснований, солей. В зависимости от свойств и структуры растворителя одно и то же вещество может быть неэлектролитом, сильным или слабым электролитом, кислотой или основанием или же вовсе не проявлять кислотно-основных свойств. [24]
 |
Зависимость выхода по току этана от природы растворителя. [25] |
Выходы этана и углекислого газа приведены для относительно низких анодных плотностей тока, при которых в случае электролиза водных растворов наблюдается довольно значительное выделение кислорода, следовательно, и эффект влияния неводных растворителей особенно заметен В растворе ацетата тетрабутиламмония. [26]
Дифференцирующее действие неводных растворителей вызывает изменение соотношения в силе электролитов и объясняется специфическим действием растворителя на растворенное вещество: подавлением диссоциации кислот сильно протогенными и оснований сильно протофильными растворителями и уменьшением диссоциации под влиянием неводных растворителей с низкими значениями диэлектрической проницаемости; неравномерным изменением значений рКл и р / Св растворенных электролитов по сравнению с их значениями в водных растворах и связанным с этим резким изменением Ар / СА и Ар / Св; различным влиянием на силу слабых и сильных кислот и слабых и сильных оснований; например, сила минеральных кислот под влиянием протогенных растворителей снижается в меньшей мере, чем сила слабых кислот, а сила сильных оснований под влиянием протофильных растворителей - в большей степени, чем сила слабых оснований. [27]
Установлено, что присутствие этилового спирта в растворе не изменяет емкости активной двуокиси марганца по стронцию для раствора, соприкасающегося с воздухом. Влияние неводного растворителя сказывается лишь на параметре изотермы Ленгмюра а, характеризующем сродство иона к данному адсорбенту. [28]
В то время, как в водных растворах реакции замещения в комплексах Сг ( Ш) идут медленно, в органических растворителях ( в этаноле [108] и трибутил-фосфате [109]) реакции значительно ускоряются. Отсюда следует, что влияние неводного растворителя можно использовать при получении комплексов металлов, но необходимы более систематические исследования в этой области. [29]
Бургера проанализированы опубликованные данные о влиянии неводных растворителей на протекающие в них реакции, сделана попытка классифицировать такие растворители в свете сегодняшних представлений об их физико-химических свойствах. Книга написана с учетом того, что большинство реакций в неводных растворителях - это фактически реакции комплексообразования. И в определенном смысле представление материала в книге является новаторским, с позиций применения понятий современной координационной химии для описания реакций в неводных средах. [30]
Страницы: 1 2 3