Влияние - химическая реакция
Cтраница 3
Учитывая отмеченное выше, представляет интерес рассмотреть упрощенный способ оценки влияния химической реакции в потоке охладителя на температурное поле пористой стенки. [31]
Они наиболее хорошо разработаны и удобнее других при использовании для оценки влияния химической реакции. При этом вопрос о том, какая из трех указанных моделей ближе к реальным условиям, гораздо менее важен, чем вопрос, какая из них дает наиболее точную количественную оценку влияния химической реакции на скорость процесса. Как видно из дальнейшего, предсказания, основанные на всех трех моделях, весьма близки, если не считать влияния на скорость абсорбции коэффициентов диффузии растворенного газа и реагентов. [32]
Однако подавляющему большинству авторов, по-видимому, не удалось четко определить пределы влияния химических реакций на чисто фазовые превращения, разграничить кинетику и равновесие химических взаимодействий от кинетики и равновесия фазовых переходов. [33]
При малых значениях параметра а2 ( 0 5 и менее) k l, т.е. влияние химической реакции незначительно, и процесс может приближенно рассматриваться как физическая абсорбция. [34]
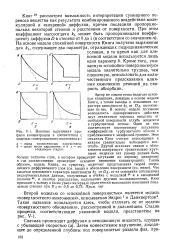 |
Влияние нарушения профиля концентрации в соответствии с моделью поверхностного омоложения. [35] |
Кроме того, указанную спокойно-поверхностную модель значительно труднее, чем пленочную, использовать для количественного предсказания влияния химических реакций ( на скорость абсорбции. [36]
Такая согласованность теоретических и экспериментальных результатов может быть объяснена очень малой толщиной диффузионного пограничного слоя, устанавливающейся под влиянием химической реакции, и является подтверждением решения (5.15) в случае пленок очень малой длины. [37]
При выполнении таких расчетов обычно следует принимать во внимание одновременный перенос тепла и массы путем вынужденной конвекции под влиянием химической реакции как в газовой, так и в жидкой фазе. Решение такой задачи, безусловно, связано с большими трудностями, особенно из-за очень сложной геометрии поверхности раздела газ - жидкость. Эта геометрия зависит от формы элементов насадки, которые с целью повышения скоростей переноса массы и тепла делаются такими, чтобы увеличивалась поверхность раздела и усиливалась турбулизация потока. Поскольку точный математический анализ процесса поглощения газа в насадочной колонне невозможен, необходимо создать модель, которая будет адекватно аппроксимировать перенос тепла и вещества в насадочном газовом абсорбере. [38]
Рассмотрим случай одной модельной эндотермической реакции, протекающей в объеме без протока газа; исследование этой системы позволяет изучить влияние химической реакции на функцию плотности вероятности пульсаций температуры и концентраций. [39]
Первый из них - это случай очень быстрой последующей реакции; система все время находится в состоянии равновесия, и влияние химической реакции по сравнению с простым диффузионным процессом проявляется только в том, что кривые восстановления смещены в направлении положительных потенциалов. [40]
В общем случае, особенно для открытых систем, следует применять более полную формулу ( 35), второе слагаемое которой характеризует влияние химической реакции на температуру плавления. Например, если имеет место очень сильная тенденция к комплексообразованию ( К велико), то достаточно совсем малых изменений активности ( или концентрации) комплексооб-разующего компонента, чтобы вызвать заметный сдвиг фазового равновесия. В подобных случаях нетрудно наблюдать процесс плавления или кристаллизации в изотермических условиях. И наоборот, если К мало, требуются большие изменения активности, чтобы понизить температуру плавления. Однако в непосредственной близости точки плавления малые изменения ас могут все же в сильной степени изменять концентрацию свободных и связанных компонентов, вследствие фазового перехода. [41]
 |
Схема поташной очистки конвертированного газа от двуокиси углерода. [42] |
Математическая модель хемосорбции двуокиси углерода поташным раствором, описывающая структуру потоков жидкости и газа в насадке, массовом ен между жидкой и газовой фагами, влияние химической реакции на скорость массообмена, была составлена на основе принципа деления аппарата на кинетические зоны / 5 / в зависанюсти от взаимодействия газовой и жидкой фаз по высоте колонны с изменение концентрации раствора. [43]
Кроме того, Корейцу пришлось принять также следующие ограничения: 1) поля пульсаций скорости и концентрации реагента изотропны и пространственно однородны; 2) влияние химической реакции на гидродинамические характеристики системы пренебрежимо мало; 3) коэффициент скорости химической реакции инвариантен к пространству и времени. Следовательно, при обычном статистическом подходе число неизвестных превышает, как правило, число уравнений, п для нахождения решения требуется введение дополнительных предположений о свойствах более высоких моментов. [44]
Требуется решить два дифференциальных уравнения второго порядка в частных производных для температуры и концентрации горючего, каждое из которых включает множитель Арре-ниуса первого порядка, определяющий влияние химической реакции. Эти уравнения решаются методом, аналогичным тому, которым пользовался Гольдштейн при получении решения для потока в следе. [45]
Страницы: 1 2 3 4