Влияние - химическая реакция
Cтраница 4
Если скорость реакции невелика ( как в рассматриваемом примере), появляется дополнительное сопротивление поверхности раздела фаз, выражаемое членом 1 / / гь Если пренебречь влиянием химической реакции и рассчитывать общий коэффициент массопередачи / Сл, учитывая только kR и kE, это приведет к результатам, не соответствующим опытным данным. Мурдох и Пратт79 рассмотрели также случай, когда на поверхности контакта фаз протекает реакция не первого порядка и т не является постоянной величиной. [46]
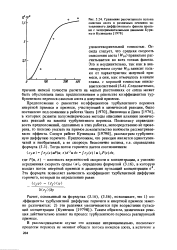 |
Сравнение рассчитанного потока окислов азота в различных сечениях затопленного диффузионного факела пропана с экспериментальными данными Бури-кои Кузнецова [ 1978. [47] |
Предположение о равенстве коэффициентов турбулентного переноса инертной примеси и примеси, участвующей в химической реакции, было поставлено под сомнение в работах Чанга [1970], Вил юно в а и Дика [1976], в которых развиты полуэмпирические методы описания влияния химических реакций на законы турбулентного переноса. Поскольку справедливость предположений, сделанных в этих работах, непосредственно не проверена, то полезно указать на прямое доказательство важности рассматриваемого эффекта. Следуя работе Кузнецова [19796], рассмотрим турбулентную диффузию горючего. [48]
Во втором случае, когда скорости реакций велики по сравнению со скоростями диффузии и конвекции, согласно уравнению ( 15 - 9) состав смеси прежде всего определяется членом, учитывающим источник массы определенного компонента. Влияние химических реакций проявляется только через физические свойства смеси, представленные в уравнениях энергии, движения и сплошности. Эти уравнения аналогичны соответствующим уравнениям для однородной среды. [49]
При этом для простоты изменениями концентраций, имеющихся в избытке реагирующих веществ, пренебрегают, причем концентрации включают в константы скорости и равновесия. Влияние химической реакции учитывают введением соответствующих выражений для скорости химической реакции в уравнения закона Фика обычным для проблем такого типа способом и при помощи преобразований Лапласа находят выражения для поверхностной концентрации, которые затем подставляют в уравнения для абсолютной скорости процесса переноса электрона. [50]
Во втором случае, когда скорости реакций велики по сравнению со скоростями диффузии и конвекции, согласно уравнению (15.9) состав смеси прежде всего определяется членом, учитывающим источник массы определенного компонента. Влияние химических реакций проявляется только через физические свойства смеси, представленные в уравнениях энергии, движения и сплошности. Эти уравнения аналогичны соответствующим уравнениям для однородной среды. [51]
Однако при определенных условиях потери корреляции за счет химических изменений могут сравниться с потерями при распаде пульсаций и масштаб турбулентности существенно изменится. Такого рода влияние химических реакций можно проследить при спаде уровня ионизации в турбулентном пламени, когда рекомбинационные процессы с участием натрия или хрома медленны, а быстрая рекомбинация электрона и иона Н30 полностью определяет кривую функции корреляции. [52]
Страницы: 1 2 3 4