Влияние - полярный фактор
Cтраница 2
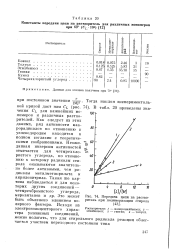 |
Передача цепи на растворитель при полимеризации стирола [ 43J. [16] |
Как следует из этих данных, ряд активности макрорадикалов по отношению к углеводородам находится в полном согласии с теоретическими соображениями. Неожиданная инверсия активностей отмечается для четыреххло-ристого углерода, по отношению к которому радикалы стирола оказываются значительно более активными, чем радикалы метилметакрилата и акрилонитрила. Такая же картина наблюдается и для некоторых других соединений - четырехбромистого углерода, меркаптанов и др. Это может быть объяснено влиянием полярного фактора. [17]
Более типичны случаи ослабления свободных радикалов за счет втягивания электрона в сопряженных системах. К числу последних прежде всего относятся радикалы аллилыюго типа, в которых смещающее влияние двойной пшзл на сопряженный с ней неспаренный электрон влечет за собой резкое падение активности свободного радикала. Те те соображения вполне применимы к объяснению причин, низкой активности бензилыгого свободного радикала. В согласии с высказанной точкой зрения о влиянии полярного фактора на реакционноспособность свободных радикалов находится также высокая активность таких радикалов, как фенил и атом водорода, для которых поляризация, подобно метальному радикалу, практически отсутствует. [18]
Таким образом, приведенные выше факты показывают, что благодаря взаимосвязи зарядовой и спиновой плотностей неспаренного электрона последняя может служить критерием реакционной способности феноксильных радикалов. Это позволяет предвидеть возможные направления радикальных реакций, предсказывать строение и соотношение конечных продуктов. Естественно, что при этом необходимо учитывать полярные и стерические эффекты заместителей, которые часто вызывают аномальное, на первый взгляд, течение реакций. Большую информацию могут дать результаты, полученные при использовании корреляционных уравнений, отражающих влияние полярных факторов на реакционную способность мо-лекул и радикалов. Так, при исследовании реакции а ос-дифенил-пикрилгидразила с различными фенолами было показано 15в - 157, что с увеличением электроноакцепторности заместителей в феноле константа скорости гомолитического отрыва атома водорода от гидроксильной группы фенола уменьшается. [19]
Из этого следует, что самой медленной стадией является стадия, соответствующая реакции радикала, обладающего наибольшей энергией резонанса. Они рассматривают энергетические параметры, определяющие реакционную способность радикала Ра и мономера Qa, как величины, эквивалентные соответствующим членам, описывающим энергию резонанса в приведенных выше уравнениях. Кроме того, они вводят новую важную величину - электростатический параметр е, которая характеризует влияние полярных факторов на энергию активации. Это эквивалентно влиянию полярных факторов на кривую отталкивания Е3 в рассмотренном выше методе. [20]
Хотя отщепление ( З - протона и перенос а-электрона при Е2 - элиминировании и происходят согласованно, эти стадии не точно синхронны: их несинхронность определяется зарядом и степенью ненасыщенности переходного состояния. Эта мысль была высказана Ханхартом и автором [2] в 1927 г., однако свое развитие она получила лишь недавно и наиболее четко - в обзоре Бан-нета [62], опубликованном в 1962 г. Она имеет стереохимическую подоплеку, поскольку стереоспецифичность Е2 - реакций зависит от степени сцепленно-сти изменений связей: при наибольшей степени сцепленности этих стадий обе связи рвутся приблизительно синхронно, а при ослаблении степени сцепленности разрыв одной связи сильно опережает разрыв другой. ElcB, при котором перенос протона происходит на отдельной предварительной стадии, и при механизме Е1, при котором аналогичным образом происходит полный электронный перенос. Можно представить, что между этими предельными случаями находится область различных механизмов Е2, в которой изменение связей происходит хотя и согласованно, но может иметь место отклонение от точной синхронизации в любом направлении и поэтому изменяться влияние полярных факторов на скорость. В предыдущем разделе были приведены данные, показывающие, что если изменение строения достаточно ацидифицирует ( i-протон, то в реакциях цик-логексана и других соединений может происходить ifwc - элиминирование, хотя эти реакции и сохраняют Е2 - характер. В этих случаях можно уверенно считать, что Е2 - механизм отклоняется в сторону механизма ElcB с преобладанием отщепления протона в степени, которая позволяет происходить уае-элиминированшо, если ацидифицированный протон находится в цис-положении. [21]
Из этого следует, что самой медленной стадией является стадия, соответствующая реакции радикала, обладающего наибольшей энергией резонанса. Они рассматривают энергетические параметры, определяющие реакционную способность радикала Ра и мономера Qa, как величины, эквивалентные соответствующим членам, описывающим энергию резонанса в приведенных выше уравнениях. Кроме того, они вводят новую важную величину - электростатический параметр е, которая характеризует влияние полярных факторов на энергию активации. Это эквивалентно влиянию полярных факторов на кривую отталкивания Е3 в рассмотренном выше методе. [22]
Страницы: 1 2