Влияние - электронный эффект - заместитель
Cтраница 1
Влияние электронных эффектов заместителей на скорость термического распада алкилпероксидов, как правило, мало. [1]
Влияние электронных эффектов заместителей на соотношение продуктов С - и О-метилирования может быть объяснено с позиции мягких и жестких кислот и оснований. Как в эфире, так и в метил бензолсульфонате повышение донорных свойств заместителя при водит к увеличению мягкости реакционных центров и, как след ствие, к увеличению доли продукта С-метилирования. [2]
В общих чертах влияние электронных эффектов заместителей на термодинамическую и кинетическую кислотность карбокислот аналогична их влиянию в рассмотренных выше классах кислот: кислотность увеличивается под влиянием роста электроотрицательности и - R - xa - рактера заместителей. Однако в случае карбокислот влияние заместителей не исчерпывается указанными факторами. Дело в том, что при диссоциации карбокислоты происходит изменение состояния гибридизации углерода в реакционном центре во всех случаях, когда кислотные свойства карбокислоты усилены присутствием - - заместителей. [3]
Кроме того, влияние электронных эффектов заместителей в субстрате в большинстве случаев значительно сильнее проявляется в реакциях мономолекулярного замещения. [4]
Однако в связи с влиянием электронных эффектов заместителей зависимость между vH и п в ряде случаев носит нелинейный характер. [5]
Таким образом, здесь преобладает влияние электронного эффекта заместителей. [6]
Как и следовало ожидать, влияние электронных эффектов заместителей на относительную стабильность а-комплексов значительно выше, чем в случае я-комплексов. [7]
В ряде случаев при гидролизе органоксисиланов отчетливо проявляется влияние электронных эффектов заместителей. Примером этого являются константы скорости основного и кислотного гидролиза серии пара - и л ега-за мешенных триэтилфеноксисила-яов. [8]
С развитием физической органической химии рассмотренные выше качественные представления о влиянии электронных эффектов заместителей на реакционную способность получили количественную интерпретацию. [9]
Так как электронное строение ароматического кольца меняется незначительно ( можно провести аналогию между этими комплексами и комплексами с переносом заряда), пои образовании л-комплексов не происходит существенных изменений в спектрах, не наблюдается увеличения электрической проводимости. Влияние электронных эффектов заместителей в ароматическом кольце на стабильность л-комплексов сравнительно невелико, так как перенос заряда в л-комплексах мал. [10]
Так как электронное строение ароматического кольца меняется незначительно ( можно провести аналогию между этими комплексами и комплексами с переносом заряда), при образовании я-комплексов не происходит существенных изменений в спектрах, не наблюдается увеличения электропроводности. Влияние электронных эффектов заместителей в ароматическом кольце на стабильность я-комплексов сравнительно невелико, так как перенос заряда в я-комплексах мал. [11]
С формальной точки зрения этот механизм подобен механизму Рг. В рамках общего изучения сравнительной чувствительности ИК-спектроскопических параметров к влиянию электронных эффектов заместителей такое поведение замещенных ацетиленов мы считаем аномальным и исключим соответствующие соединения из дальнейшего рассмотрения. [12]
Высокая чувствительность интенсивности ряда полос ИК-спектров к проявлению электронных эффектов различной природы определяет перспективность использования этой величины не только для оценки суммарного электронного влияния гетероатомных заместителей, характеризуемого о - и ( Г - - константами, но и для выделения из него / - и / И-составляю-щих. Особый интерес в указанном отношении представляют исследования интенсивностей полос, обусловленных колебаниями СН - и СС-групп ароматического кольца. Однако при количественном изучении хода изменений интенсивности этих полос под влиянием электронных эффектов заместителей приходится сталкиваться с большими трудностями, чем в рассмотренном ранее случае колебаний СН3 - групп ( 1, 2 ], так как интенсивность ароматических полос мало характеристична, а строгая теория нехарактеристичных по интенсивностям колебаний сложных молекул разработана явно недостаточно. Настоящая работа и посвящена этому направлению исследований, а именно: изучению зависимости интенсивности полос колебаний ароматических СН-связей и скелетных колебаний кольца от характеристик электронного строения ароматических и особенно гетероароматических молекул. [13]
Электронные эффекты заместителей, оцененные как качественно, так и количественно, на основе квантовохимических расчетов отражают влияние заместителя на энергию связи протона в изолированной молекуле в статических условиях и сопоставимы с изменением энтальпии ионизации в газообразном состоянии при абсолютном нуле. Кислотная диссоциация веществ протекает в растворе с участием растворителя; константы кислотной диссоциации обычно определяют при 25 С. Величины констант диссоциации отражают изменение стандартного изобарно-изотермического потенциала AG при диссоциации в растворе. В ходе кислотной диссоциации устанавливается динамическое равновесие между протонированной и депротонированной формами, поэтому влияние электронных эффектов заместителей следует изучать на обеих формах. Отсюда можно заключить, что корреляция электронных эффектов лиганда с кислотными свойствами комплексов не достаточно строга. Все же такого рода сопоставления могут быть сделаны при соблюдении ряда условий: 1) если производить относительное сравнение кислотных свойств в серии однотипных соединений с близкими изменениями энтропии диссоциации; 2) если в выбранной серии вклад гидратационного члена в величину Д7 примерно постоянен. При этом одна из кислот принимается за стандарт и оценивается изменение AG диссоциации других кислот по отношению к данному стандарту. [14]
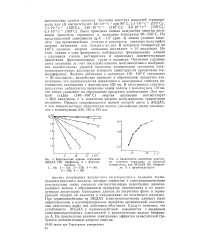 |
Кинетические кривые термолиза ЭНДАХ ПК бисфенола А с формальдегидом, С.| Зависимость изменения константы скорости термолиза от обратной температуры для ЭНДАХ ПК бисфенола А с формальдегидом. [15] |
Страницы: 1 2