Влияние - ароматическое ядро
Cтраница 1
Влияние ароматического ядра на степень ионизации гидроксильного водорода усиливается при введении в ядро галогенов или нитро-групп ( ср. [1]
Влияние ароматических ядер на распределение интенсивностей в масс-спектре, рассмотренное выше на примере различных производных дифенила, особенно четко проявляется в масс-спектрах полициклических ароматических углеводородов с конденсированными ядрами. [3]
Влияние ароматического ядра на степень ионизация гидроксильного водорода усиливается при введении в ядро галоидов или нитрогрупп ( ср. [4]
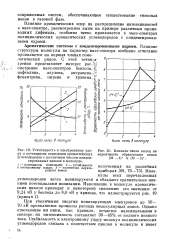 |
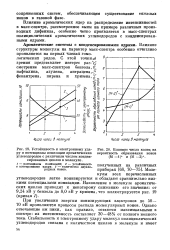
Устойчивость к электронному удару и потенциалы ионизации ароматических углеводородов с различным числом конденсированных циклов в молекуле.| Влияние числа колец на. [5] |
Влияние ароматических ядер на распределение интенсивностей в масс-спектре, рассмотренное выше на примере различных производных дифенила, особенно четко проявляется в масс-спектрах полициклических ароматических углеводородов с конденсированными ядрами. [6]
Влияние ароматического ядра на диссоциативную ионизацию гидроароматических соединений хорошо иллюстрируется распадом насыщенного кольца молекул 1 - и 2 тиатетралинов. [7]
При окислении ал-килбензолов влияние ароматического ядра сказывается как на повышении реакционной способности соседнего с ним атома углерода боковой цепи, так и на стабильности образующихся гидроперекисей. Реакция их образования протекает в жидкой фазе уже при 100 - 120 ЧС. Наиболее стабильны гидроперекиси вгор-алкилбензолов, что определяется наличием третичного углеродного атома. [8]
Это явление Файгль объясняет влиянием ароматического ядра. [9]
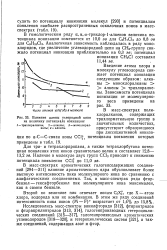 |
Влияние длины углеродной цепи на величину потенциала ионизации. [10] |
В масс-спектрах ароматических галогенсодержащих соединений [294-311] влияние ароматического ядра обусловливает более высокую интенсивность пика молекулярного иона по сравнению с алифатическими соединениями. Так, в масс-спектрах ряда фтор-бензол - гексафторбензол пик молекулярного иона максимален, как в самом бензоле. [11]
В отличие от спиртов фенолы в не слишком разбавленных водных растворах обнаруживают явную кислую реакцию в результате протонизирования атома водорода гидроксильной группы под влиянием ароматического ядра, которое несколько оттягивает электроны атома кислорода. Наиболее резко выражен кислотный характер у пирогаллола, пирокатехина и нафтолов. Однако нафтолы очень малорастворимы в воде и кислотность их раствора по лакмусу проявляется недостаточно отчетливо. [12]
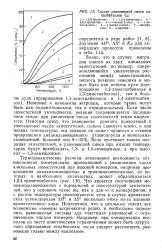 |
Состав равновесной смеси ал-килбензолов C. [13] |
Что касается соотношения мо-ноалкилзамещенных с нормальной и изоструктурой заместителей, оно в основном такое же, как и для - и изопарафиное, и с ростом температуры увеличивается, хотя в случае ароматических углеводородов ДЯ и AS0 несколько ниже из-за влияния ароматического ядра. Подчеркнем, что в реальных смесях все возможные изомеры встречаются редко, и необходимо определять равновесные составы для частных равновесий с ограниченным числом изомеров. Например, при изомеризации ксилолов по чисто кинетическим ограничениям может быть затруднено образование этилбензола; тогда следует рассмотреть равновесие только между ксилолами. [14]
Особенности химического строения вторичных меркаптанов определяют их расположение в третьем ряду агрессивности. Из-за влияния ароматического ядра вторичная сульфогидрильная группа а-фенилэтилмер-каптана обладает более высокой подвижностью и реакционной способностью по сравнению с сульфогидрильными группами циклогексилмеркаптана и 2, 4, 6-триметил - 7-тиолнонана. В последнем случае немаловажное значение имеет пространственное расположение метальных групп, затрудняющих доступ окислителей к сульфогидр илу. [15]
Страницы: 1 2