Влияние - полярная группа
Cтраница 2
 |
Влияние полярных групп. [16] |
Чем выше диэлектрическая постоянная образца, тем легче под влиянием полярных групп, введенных в цепь сополимера, осуществляется адсорбция влаги и диссоциация на ионы и в результате тем выше электропроводность. [17]
За последние пятьдесят лет достигнуты большие успехи в количественной оценке влияния полярных групп. Эти данные получены при изучении систем, в которых пространственный эффект оставался постоянным или не играл заметной роли. Лучшим примером такого исследования является большая серия работ, посвященных изучению мета - и геара-дизамещенных производных бензола, для которых определение констант Q и а, по Гаммету, дает хорошие результаты и возможность в определенных пределах предсказывать ход реакции. [18]
В случае ионогенных ПАВ эффекты дегидратации сохраняют свое значение, однако появляется дополнительный фактор - влияние заряженных полярных групп молекул ПАВ, которые оказывают разрушающее действие на структуру воды. [20]
Метод позволяет объяснить наблюдаемые закономерности в хроматограф, спектрах и может быть также применен для определения влияния концевых полярных групп и сопряжения на величины удерживания. [21]
Такая закономерность, по-видимому, связана, с одной стороны, с влиянием длинных алифатических цепей, увеличивающих эластичность композиции, а с другой - с влиянием функциональных полярных групп на величину адгезии. Сочетание этих двух факторов приводит к повышению адгезионных свойств полимерных композиций только при некоторых благоприятных для данной композиции соотношениях компонентов. [22]
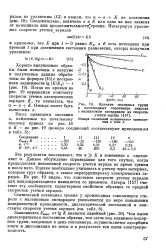
Соединения, характеризующиеся переломом в нижней чаоти кри вой F-А, типичным примером чего может служитьлинпя ABD ( рис. 8), обнаруживают это аномальное поведение, повидимому, вследствие влияния полярной группы в конце цепи, так как положение участка BD изменяется от группы к группе, но остается постоянным для каждой данной группы. Площадь D, очевидно, характеризует плотную, но не сжатую упаковку активных головных групп. Возможно, что это является следствием сольватации ( стр. [23]
Бекер и Фуллер [134] показали, что процесс перехода расплавленного полиэфира в твердое состояние происходит с фазовым переходом, подобным тому, какой наблюдается у низкомолекулярных органических вещестр, При этом способность полиэфиров к кристаллизации оказывается тем большей, чем меньше их молекулярный вес и чем меньше влияние полярных групп. На рис. 134 - 138 приведены кривые охлаждения ряда полиэфиров. На рис. 139 показана кривая нагревания полиэтиленсукцината. Фазовый переход, означающий, что, по крайней мере, часть образца кристаллизуется самопроизвольно, найден для ряда полиэфиров, как это-показано на приведенных кривых, из которых ясно видно прекращение падения температуры в момент кристаллизации. Замечено, что полидисперсные полимеры кристаллизуются медленнее. Это оправдывает сегментный механизм кристаллизации полимеров. [24]
Эта частота постоянна в такой же степени, как и частоты в случае уже рассмотренных типов двойных связей. Влияние полярных групп на частоту по существу является таким же, как и у виниловых соединений. [25]
Наличие большого числа полярных групп приводит к снижению оптической чувствительности. В этом отношении влияние полярных групп противоположно тому влиянию, которое они оказывают на температуру стеклования. [26]
Объяснение такого увеличения растворяющей способности растворителя нельзя отнести только за счет повышения общей полярности системы из-за образования наведенного диполя в молекуле бензола, так как при добавлении полярного растворителя в таком же количестве, как бензола, не получается такого эффекта, хотя полярность растворителя выше, чем индуцированный диполь молекулы бензола. По-видимому, молекулы бензола под влиянием полярной группы растворителя приобретают некоторый индуцированный дипольный момент, в результате чего происходит ориен-тационное взаимодействие их с молекулами полярного растворителя ( квадруполь), ведущее к усилению дипольного момента системы. Одновременно с этим в присутствии в таком ассоциированном комплексе бензольного ядра усиливается его дисперсионный эффект. [27]
Применяя такой же метод оценки, Лутцу194 нашел, что предел прочности при растяжении и нагрузка, требующаяся для достижения относительного удлинения на 100 % олигомерных метакрилатов спиртов Q, Gt, С8, снижаются с удлинением спиртового радикала или с увеличением степени полимеризации. В более высокомолекулярных соединениях, и вероятно также в соединениях с разветвленной структурой, влияние полярных групп сказывается еще в меньшей степени. [28]
Так как полярные группы, определяющие растворимость аминокислот, одинаковы для различных аминокислот, коэффициенты распределения аминокислот различаются незначительно, и, следовательно, их разделение становится трудной задачей. При ацетидаровании [172] или образовании пипсиль-ных производных ( / г-иодфенилсульфоншшроизводные) [94] фракционирование облегчается за счет уменьшения влияния полярных групп. Хроматографические методы значительно более эффективны по разрешающей способности, но они ограничены возможностью выделения сравнительно небольших количеств веществ. Успешное применение метода противоточного распределения зависит в значительной степени от подходящего выбора двухфазной системы растворителей. Кроме того, применение этого метода ограничивается возможностью разделения веществ низкого молекулярного веса ( 10 000), за исключением тех случаев, когда пептиды обладают большой устойчивостью к денатурации. В присутствии большинства двухфазных систем растворителей, как правило, легко происходит денатурация белков. Однако при нахождении благоприятных условий противоточное распределение-имеет преимущество по сравнению с другими методами, так как при этом возможно рассчитать коэффициенты распределения компонентов, которые могут быть установлены с большой точностью. Профиль кривой распределения дает хороший критерий чистоты вещества. [29]
Как видно из табл. 43, в гомологических рядах данной группы соединений зависимость между молекулярным весом и летучестью с водяным паром обратная: с увеличением молекулярного веса возрастает и летучесть с паром. Это может быть объяснено тем, что при увеличении углеводородного остатка увеличивается и его влияние на свойства молекулы в целом, а влияние полярной группы уменьшается. По той же причине введение в молекулу второй полярной группы вызывает резкое понижение летучести с водяным паром. Так, хлоруксусная кислота в 14 раз менее летуча, чем уксусная кислота; антраниловая кислота в 15 раз менее летуча, чем бензойная кислота и в 290 раз менее летуча, чем анилин; n - нитрофенол в 388 раз менее летуч, чем фенол, а эти-лендиамин в 1000 раз менее летуч, чем этиламин. [30]
Страницы: 1 2 3 4