Влияние - двуокись - углерод
Cтраница 1
Влияние двуокиси углерода на межфазное натяжение водонефтяных систем сильно зависит от наличия природных ПАВ в нефти. Для конкретных условий поверхностное натяжение может быть определено экспериментально. [1]
 |
Влияние концентрации двуокиси углерода. [2] |
Влияние двуокиси углерода оказалось совершенно различным для образцов, содержащих и не содержащих добавок. Как видно из рисунка, кинетические кривые для образца 1, не содержащего добавок, при малом содержании двуокиси углерода в исходном газе практически совпадают. При большем содержании двуокиси углерода в исходной, газовой смеси ( 10 % и выше) в диффузионной области реакция несколько замедляется. Однако значения максимальных скоростей реакции и в этом случае остаются практически постоянными. [3]
Влияние двуокиси углерода на нижний концентрационный предел несколько иное; здесь наблюдается заметное смещение нижнего предела вправо, навстречу смещению верхнего предела. Это объясняется тем, что двуокись не является полностью инертным газом. Для подавления воспламенения ( полной флегматизации смеси) необходимы значительные количества присадок. [4]
Это влияние двуокиси углерода аналогично рассмотренному раньше для взаимодействия аммиака с хлорпроизводными ( стр. [5]
Во избежание влияния двуокиси углерода воздуха на электропроводность вместо дистиллированной воды для поглощения НС1 применяют слабые растворы соляной кислоты. [6]
Тимолфталеин под влиянием двуокиси углерода изменяет синюю окраску на желто-оранжевую. Носителем реагента является окись алюминия, содержание СО2 определяют по калибровочному графику. [7]
Во время анализа влияние двуокиси углерода воздуха должно быть исключено. [8]
 |
Зависимость производительности цинк-хромового катализатора. [9] |
Мнения исследователей о влиянии двуокиси углерода на активность цинк-хромового катализатора до последнего времени были противоречивы. В одних случаях указывалось, что при наличии двуокиси углерода даже в небольших количествах снижается скорость образования метанола, повышается содержание воды в продукте и увеличивается расход газа. По другим данным, предварительная обработка катализаторов двуокисью углерода может повышать их аисгивность. В промышленных условиях синтеза вследствие восста новления двуокиси углерода концентрация ее в циркуляционном газе в зависимости от отношения Н2: СО колеблется от 0 3 до 1 0 объемл. [10]
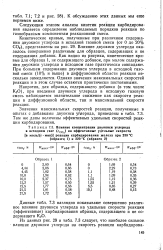
В табл. 20 приведены данные о влиянии двуокиси углерода в исходной смеси на активность силикагеля и активного угля по изобутану и изопентану. [11]
Самедар и Рза-Заде [11], которые исследовали влияние двуокиси углерода на MoS2, нашли, что при 200 - 500 С MoS2 медленно окисляется, превращаясь в МоО2, а полностью окисляется только через 54 ч при 900 С. [12]
Из описания патента нельзя сделать заключения, насколько важным является влияние двуокиси углерода. Реакцию ведут следующим образом: дифенол кипятят в течение 4 - 6 час. Недостатком этого способа, так же как и ранее известного, является невозможность получить полиглицидные зфиры желаемой степени полимеризации. Кроме того, регенерация растворителя из большого количества воды экономически невыгодна. [13]
Из описания патента нельзя сделать заключения, насколько важным является влияние двуокиси углерода. Реакцию ведут следующим образом: дифенол кипятят в течение 4 - 6 час. Недостатком этого способа, так же как и ранее известного, является невозможность получить полиглицидныезфирыжелаемой степени полимеризации. Кроме того, регенерация растворителя из большого количества воды экономически невыгодна. [14]
Ускорение разложения гипохлоритов ( потеря ими активного хлора) под влиянием двуокиси углерода объясняется вытеснением ею свободной хлорноватистой кислоты, диссоциирующей с образованием иона СЮ, который затем распадается по одной из приведенных реакций. В водных щелочных растворах гипохлориты относительно устойчивы. При щелочности 2 - 3 % растворы гипохлорита натрия могут храниться в течение 10 - 15 суток. [15]
Страницы: 1 2 3