Структура - аминокислота
Cтраница 1
 |
Каталитические группы ферментов. [1] |
Структуры аминокислот сведены в таблицу в разд. [2]
Цвиттер-ионной структуре аминокислот, даже в растворах, вполне соответствуют низкие значения констант Ка и Кь. Очевидно, что величина Ка отражает способность группы NH3 отдавать протон, а величина Къ - способность группы С00 - приобретать протон. Ситуация становится еще более сложной для тех аминокислот, которые содержат более одной карбоксильной группы или более одной аминогруппы, но в целом величины Ка и Кь для аминокислот, содержащих лишь одну амино - и одну карбоксигруппы, очень близки к соответствующим величинам для глицина. [3]
Цвиттер-ионной структуре аминокислот, даже в растворах, вполне соответствуют низкие значения констант Ка и Къ. Очевидно, что величина Ка отражает способность группы NH3 отдавать протон, а величина Кь - способность группы С00 - приобретать протон. Ситуация становится еще более сложной для тех аминокислот, которые содержат более одной карбоксильной группы или более одной аминогруппы, но в целом величины Ка и Кь для аминокислот, содержащих лишь одну амино - и одну карбоксигруппы, очень близки к соответствующим величинам для глицина. [4]
 |
Методы получения производных аминокислот для газохроматографического анализа. [5] |
Из-за бетаиновой структуры аминокислоты относятся к неиспаряющимся соединениям, и поэтому их нельзя непосредственно исследовать методом газовой хроматографии. По аналогии с анализом жирных кислот за прошедшие годы были поставлены опыты по разрушению бетаиновой структуры при помощи получения летучих производных. Химия проб в применении к аминокислотам имеет гораздо больше возможностей, чем в случае жирных кислот. [6]
 |
Методы получения производных аминокислот для газохроматографического анализа. [7] |
Из-за бетаиновой структуры аминокислоты относятся к неиспаряющимся: соединениям, и поэтому их нельзя непосредственно исследовать методом; газовой хроматографии. По аналогии с анализом жирных кислот за прошедшие годы были поставлены опыты по разрушению бетаиновой структуры при помощи получения летучих производных. Химия проб в применении к аминокислотам имеет гораздо больше возможностей, чем в случае жирных кислот. [8]
Важность изучения структур аминокислот не исчерпывается только тем, что они являются составными частями белковых молекул. [9]
Метод двумерной хроматографии позволил установить зависимость между структурой аминокислоты и положением соответствующего ей пятна на бумаге. Были подробно разработаны методы количественной хроматографии. Изучены гидролизаты бактерий, зубов, рыб, фасоли, кератина, слюны, ферментативные гидролизаты на содержание в них различных аминокислот. [10]
Метод масс-спектрометрии можно с успехом применять для установления структуры аминокислот и пептидов. [11]
Их длины близки к длинам аналогичных связей в структурах исследованных аминокислот. [12]
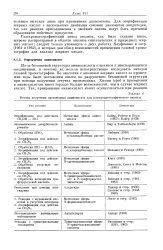
В работе [223] содержится обзор водородных связей в 28 структурах аминокислот, пептидов и родственных молекул, исследованных нейтронографиче-ским методом, и в 68 структурах, исследованных рентгеноструктурным методом; эта работа может рассматриваться как часть настоящего обзора. Мы выбрали за период 1969 - 1978 гг. те рентгеноструктурные исследования, в которых проводилось определение положений атомов водорода. Результаты анализа данных приведены в табл. 4.2. Расчеты 439 водородных связей позволили выявить среди них около 55 различных типов водородного связывания. [13]
Этот вопрос был полностью выяснен при помощи других физико-химических методов, которые бесспорно доказали ди-польную структуру аминокислот. [14]
Эфиры аминокислот в виде свободных оснований нестабильны и даже при комнатной температуре легко превращаются к дике-топиперазины, причем скорость этого превращения зависит от структуры аминокислоты и характера алкильной группы эфира. [15]
Страницы: 1 2